Jeder Stoß ein Treffer?
Weiteres
Warum gibt es eigentlich eine messbare Reaktionsgeschwindigkeit?
In Gasgemischen bei normalen Drücken und Temperaturen kann doch jedes Molekül etwa 1010-mal pro Sekunde auf ein anderes Molekül stoßen.
Weiteres
Animiertes Modell einer Reaktion auf Teilchenebene1
Aufgaben
- Benennen Sie die Annahme, die hinter der Ausgangsfrage oben steckt.
- Beschreiben Sie unter Verwendung des Modells der Teilchenkollisionen in M2, was diese Annahme außer Acht lässt.
- Geben Sie eine erläuternde Antwort auf die in M1 genannte Frage unter Verwendung von M2 und M3.
Erfolgreiche und nicht erfolgreiche Stöße auf Teilchenebene
Weiteres
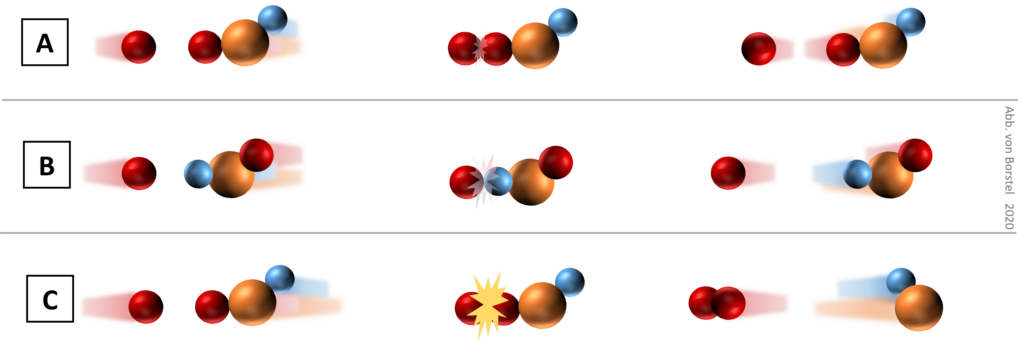
Betrachten wir einmal nicht nur die Anzahl der Stöße, sondern auch ihre Qualität. Die Teilchen müssen in der richtigen Orientierung und mit genügend hoher Geschwindigkeit aufeinandertreffen, damit eine Reaktion stattfindet. Dies zeigt das Modell in Abb. 1 für drei verschiedene Szenarien A, B und C.
Teilchen vor, während und nach der Kollision. Stoß A und Stoß B sind ineffektiv, Stoß C ist effektiv2
Die Barriere der Aktivierungsenergie
Weiteres
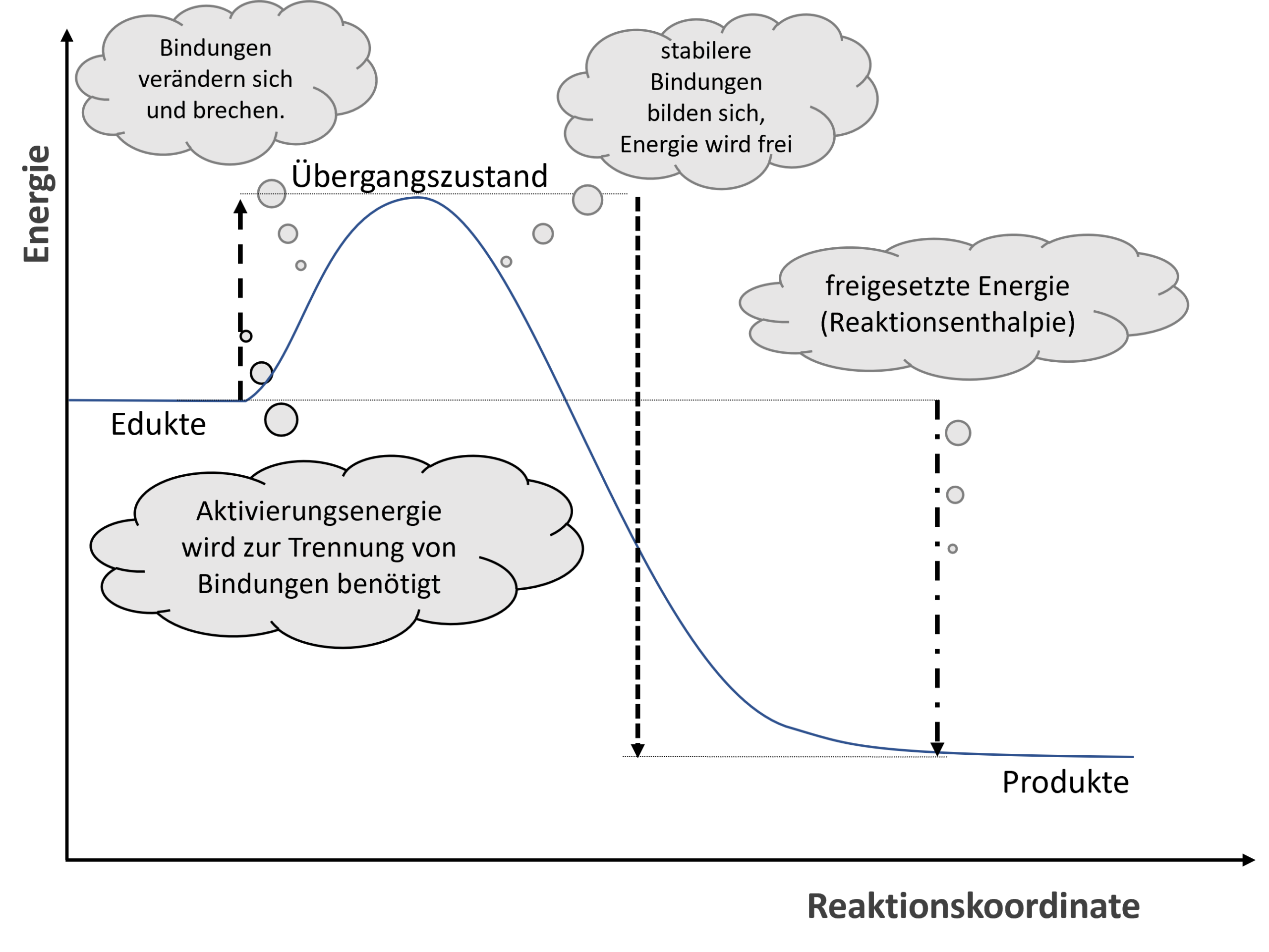
Wie Sie bereits wissen, erfolgen chemische Reaktion erst bei einer sogenannten Aktivierungsenergie (Abb. 2). Dies liegt daran, dass auf Teilchenebene Bindungen aufgebrochen werden müssen.
Die dafür notwendige Energie stammt aus der Bewegungsenergie der Teilchen beim Stoß.
Ein bereits aus der Sekundarstufe 1 bekanntes Energiediagramm.2
Bei gleicher Temperatur haben die Teilchen in einer Stoffprobe aber keineswegs die gleiche Geschwindigkeit. Sie stoßen permanent zusammen, werden gebremst und beschleunigt.
Weiteres
Es gibt also ein breites Spektrum an Geschwindigkeiten, die mit unterschiedlicher Häufigkeit auftreten. Ludwig Boltzmann hat erkannt, dass die Häufigkeitsverteilung der Geschwindigkeiten und damit Energie von Gasteilchen von der Temperatur abhängt und dies mathematisch erfasst.
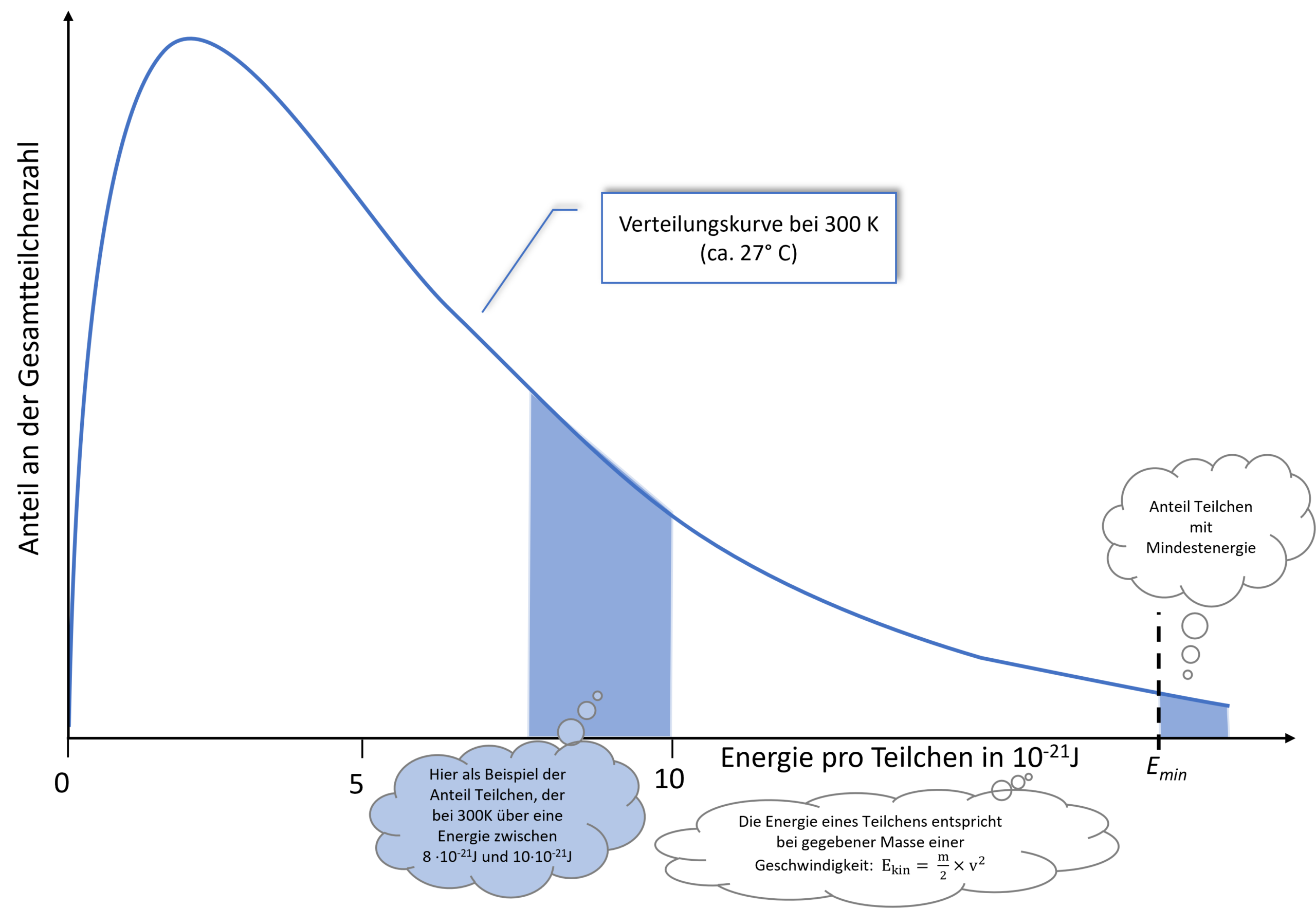
Die genauen mathematischen Zusammenhänge führen deutlich über das hinaus, was wir behandeln wollen. Aber die folgende Abb. 3 stellt dies dar und ist gut nachvollziehbar.
Die sogenannte „Maxwell-Boltzmann-Verteilung“2
Weiteres
Die Maxwell-Boltzmann-Verteilung werden wir nun einige Male nutzen. Du musst hier nicht die Mathematik dahinter kennen oder anwenden können. Aber du solltest das Diagramm so gut verstehen, dass du es als Erklärungshilfe für die Auswirkungen von Veränderungen in einer Stoffprobe nutzen kannst.
Weitergedacht
- Erläutern Sie auf Teilchenebene mit Hilfe von M4 die zu beobachtende Erwärmung einer Stoffprobe bei einer exothermen Reaktion
Alles auf einen Blick
Weiteres
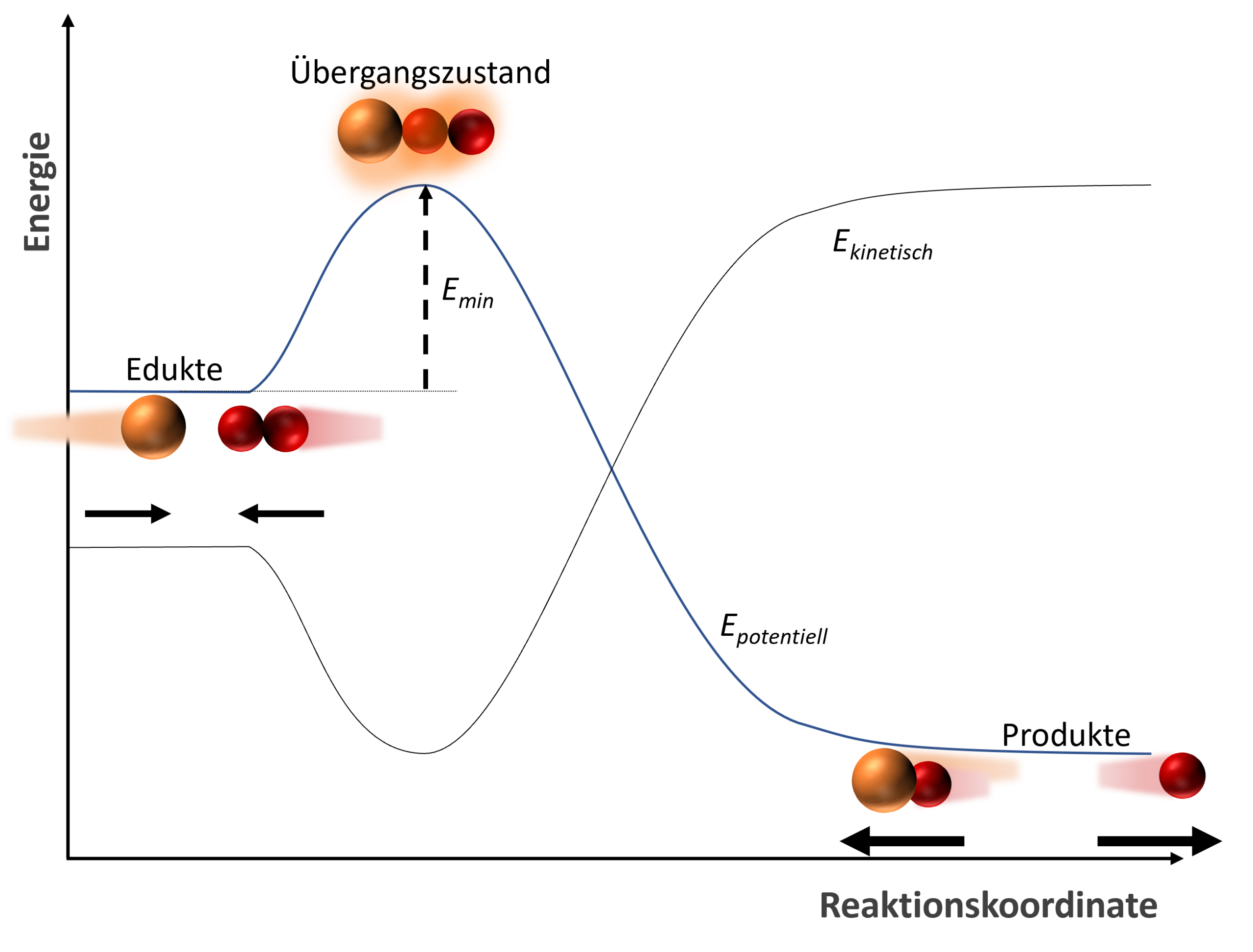
Ein etwas anderes Energiediagramm2