Wenn die Oberfläche eines Feststoffs eine Rolle für die Reaktionsgeschwindigkeit spielt, dann doch sicherlich auch die Konzentration der beteiligten Stoffe in der Lösung, oder?
Für die uns bereits bekannte Reaktion von Magnesium mit Salzsäure könnten wir das leicht im Experiment prüfen.
Aufgaben
- Stellen Sie eine begründete Hypothese zum möglichen Einfluss der Konzentration auf die Reaktionsgeschwindigkeit auf.
- Prüfen Sie Ihre Hypothese, indem Sie
- das Experiment V1 nach Anleitung oder in einer sinnvollen Variation durchführen sowie auswerten,
- oder Ausschnitte aus M2 nutzen, um die Anfangsgeschwindigkeiten der Reaktionen der unterschiedlich konzentrierten Säuren in bestimmten Zeitintervallen zu bestimmen.
- Erläutern Sie ihre Versuchsbeobachtungen mit Hilfe von M4.
Einfluss der Konzentration auf die Reaktionsgeschwindigkeit
Materialien
- Schutzbrille
- 2 Spritzen (12 mL)
- 2 Spritzen (30 mL)
- Verbinder luer-lock w-w
- Rückschlagventil luer-lock
- alternativ 3-Wegehahn zum Verschließen
- Becherglas
- 2 Klammern mit Magnet
- fakultativ zum Fixieren während der Filmaufnahme
Chemikalien
- Salzsäure (1 mol / L)
- Salzsäure (0,5 mol / L)
-
Magnesiumband, gefaltet ca. 2 cm
- wiegen!
Hinweis
Es entsteht Wasserstoff – von Zündquellen fernhalten!
Aufbau und Durchführung
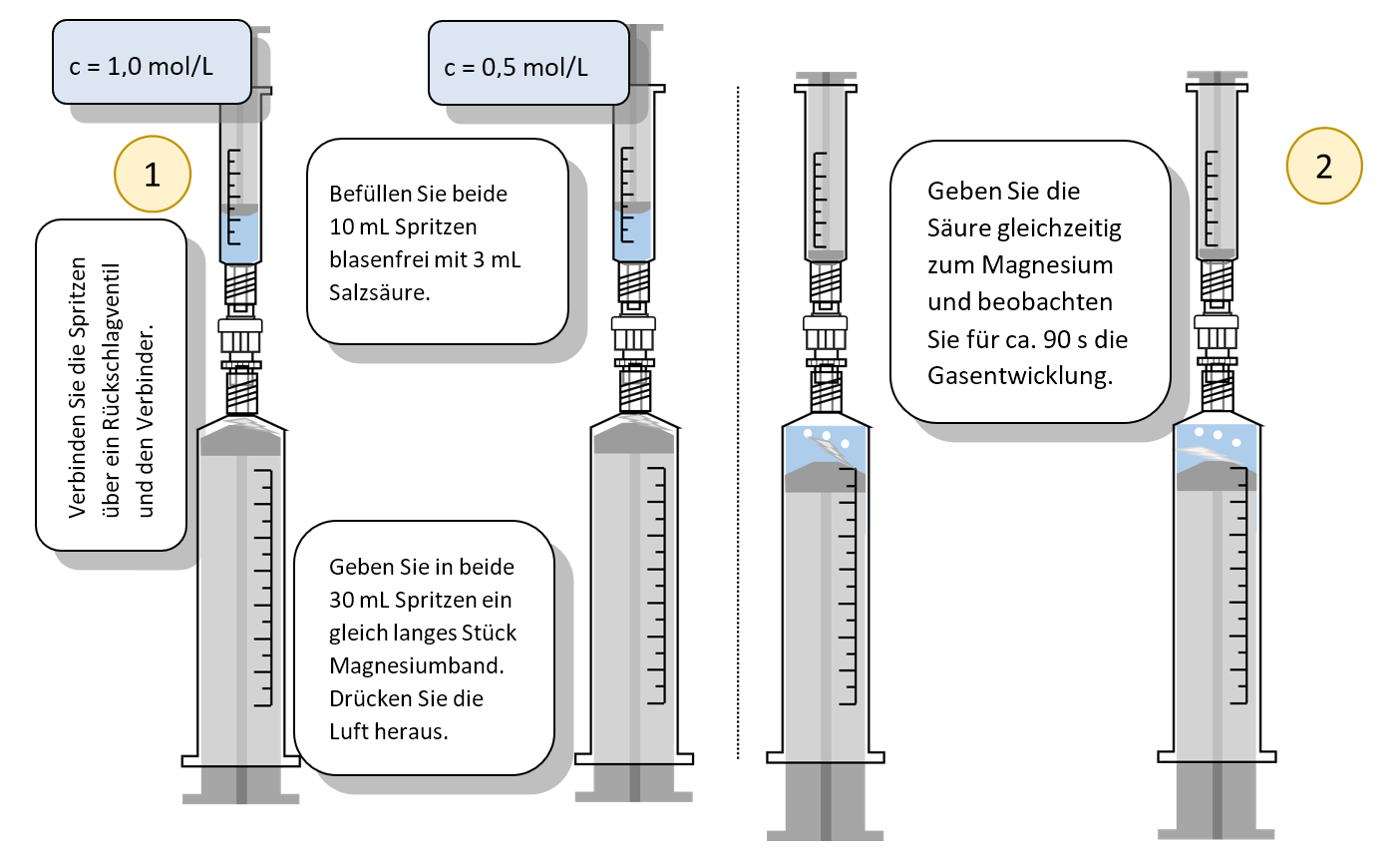
- Befüllen Sie beide kleinen Spritzen blasenfrei mit je 3 mL Salzsäure.
- Geben Sie in beide 30 mL Spritzen je ein gleich großes Stück Magnesiumband. Drücken Sie alle Luft aus den beiden Spritzen heraus.
- Verbinden Sie je eine kleine „Salzsäure-Spritze“ mit einer größeren „Magnesiumband-Spritze“ derart, dass die Säure zum Magnesium gedrückt werden kann.
- Hängen Sie die Spritzen mit einem Magnethalter auf, starten Sie eine Videoaufnahme des Experiments und geben Sie gleichzeitig in beiden Konstruktionen die Säure zum Magnesium.
- Filmen und beobachten Sie die Gasentwicklung für ca. 90 Sekunden.
Beide Reaktionen gleichzeitig starten (1) und dann beobachten (2). 1
Entsorgen und Aufräumen
-
Restliche Lösung in den Sammelbehälter für Schwermetallsalze geben. Entstandenen Wasserstoff im Abzug oder am offenen Fenster in die Luft entlassen.
-
Alle verunreinigte Labormaterialien spülen.
-
Alle Materialien an ihren Ursprungsort zurückstellen.
Alternative zum eigenen Versuch: Videografie von vier Experimenten
Weiteres
Der uns bereits bekannte Versuch wurde hier vier Mal durchgeführt. Bei jeder erneuten Durchführung variierte alleine die Konzentration der Salzsäure.
Weiteres
Zeitrafferaufnahme, [HCL] = 1,00 mol/L.1
Auswertungshilfe bei Bedarf
Für V1 oder M2
Stoßtheorie und mathematische Zusammenhänge
Die Stoßtherorie passend zu unserem Versuch mit zwei Phasen
Ein vereinfachtes, noch zu ergänzendes Modell für den Versuch könnte wie folgt aussehen:
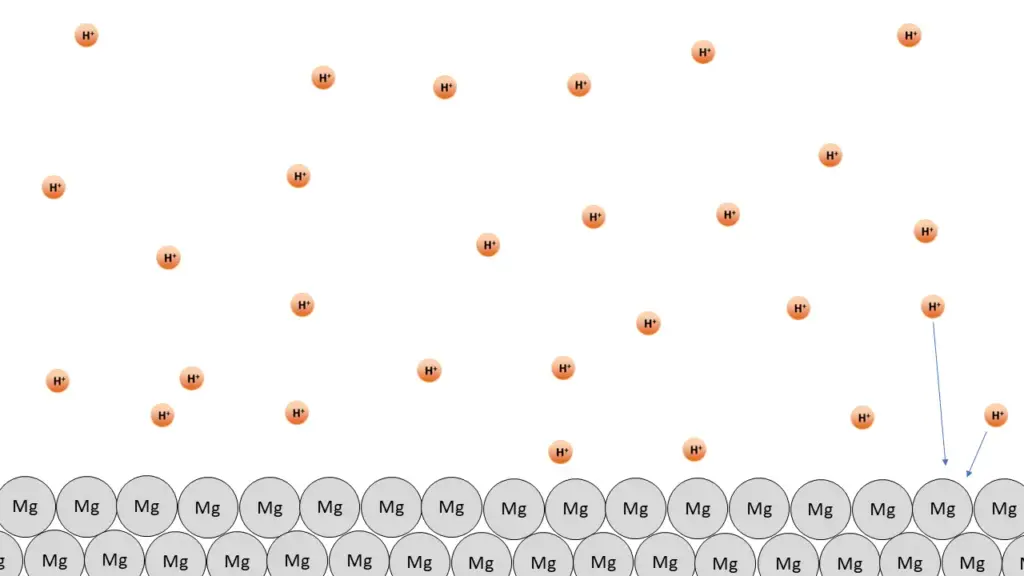
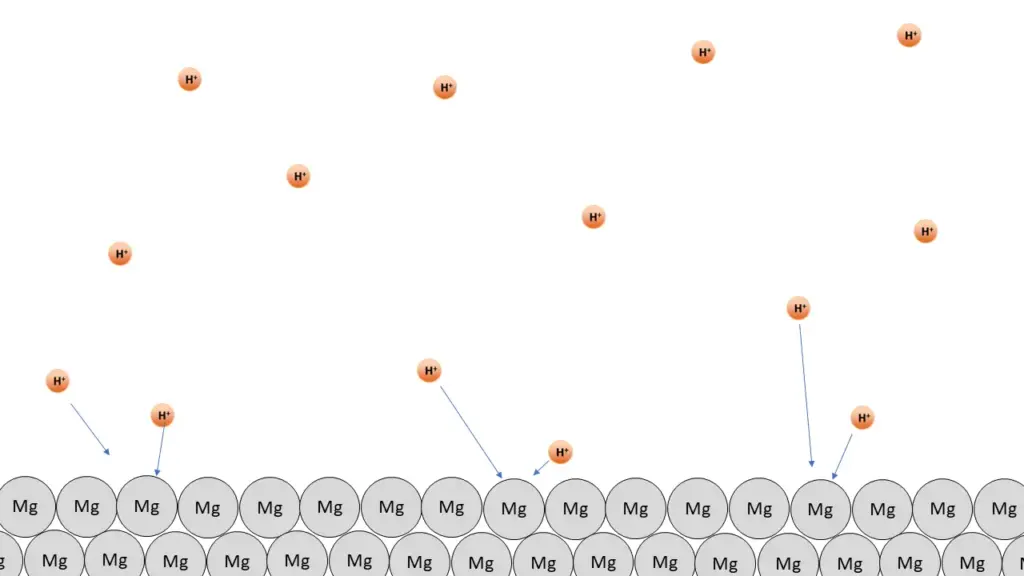
Vorlage „Halbe bzw. doppelte Konzentration“ zum Herunterladen und Ergänzen.2
Die Stoßtheorie für Reaktion in einer Lösung oder Gasphase
Die Stoßtheorie besagt, dass chemische Reaktionen erfolgen, wenn Teilchen (Atome, Ionen oder Moleküle) zusammenstoßen und ausreichend kinetische Energie besitzen, um die Aktivierungsenergie zu überwinden.
Die Erhöhung der Konzentration eines Stoffes sollte zu mehr Kollisonen führen. Mehr Zusammenstöße pro Zeiteinheit führen zu einer höheren Reaktionsgeschwindigkeit.
Mögliche Treffer in Anhängigkeit von der Teilchenanzahl.1
Mathematische Betrachtung unserers Versuchs
Bei der Reaktion von Magnesium mit Salzsäure
ist die Reaktionsgeschwindigkeit (v) direkt proportional zur Konzentration der H+-Ionen, die aus der Salzsäure (HCl(aq)) stammen. Wird also die HCl-Konzentration verdoppelt, so verdoppelt sich in der Regel auch die Geschwindigkeit der Reaktion zwischen Magnesium und den H+-Ionen.
Man kann diese Beziehung mathematisch so ausdrücken:
Dabei ist k die Geschwindigkeitskonstante, die von weiteren Faktoren wie Temperatur oder der Oberfläche des Magnesiums abhängt, [HCl] steht für die Konzentration der Salzsäure. Da diese vollständig in Wasser dissoziiert, gilt übrigens [HCl] = [H+]
Allgemeine mathematische Betrachtung
Bei vielen anderen chemischen Reaktionen in einer Lösung oder Gasphase ist es oft so, dass die Reaktionsgeschwindigkeit von der Konzentration beider (aller) Edukte abhängt. Für eine Reaktion
wird die Reaktionsgeschwindigkeit häufig durch die Gleichung beschrieben:
Wie wir sehen werden, gilt die obige Formel allerdings nicht immer!
Weiteres
Wir können an dieser Stelle auch gut mit der Maxwell-Boltzmann-Verteilung argumentieren.
Ein Blick in die Säure-Base-Chemie
- In einem Versuch werden die Anfangsgeschwindigkeiten der Reaktionen von Magnesium mit a) Salzsäure und b) Essigsäure – beide jeweils 1 molar – miteinander verglichen. Die Anfangsgeschwindigkeiten beider Versuchen unterscheiden sich deutlich. Benennen Sie einen möglichen Denkfehler, der der Annahme zugrunde liegt, dass die Anfangsgeschwindigkeiten gleich sein müssten.