Aufgaben
- Stelle mit M1 heraus, wie man Kochsalz normalerweise gewinnt
- Erkläre mit M2, was bei der Kochsalzsynthese aus den Elementen auf Teilchenebene passiert.
- Erkläre den Untertitel dieser Seite.
Wie man normalerweise Kochsalz gewinnt
Der normale Weg
Kochsalz (Natriumchlorid) würde man normalerweise auf zwei Arten gewinnen: aus unterirdischen Salzlagerstätten und aus Meerwasser.
In Salzlagerstätten liegt das Salz in Schichten vor. Es wird entweder im Bergbau abgebaut oder durch Wasser herausgelöst. Dabei wird Wasser in die Lagerstätte gepumpt, löst das Salz und es entsteht eine Salzlösung (Sole). Diese Sole wird nach oben gefördert und anschließend eingedampft, sodass festes Salz zurückbleibt.
Im Meerwasser ist Salz bereits gelöst. In warmen Regionen wird Meerwasser in flache Becken geleitet (Salinen). Durch die Sonne verdunstet das Wasser langsam, und das Salz kristallisiert aus. Die festen Salzkristalle werden dann gesammelt und weiter gereinigt.
Beide Verfahren nutzen also denselben Grundgedanken: die Ionen liegen bereits.
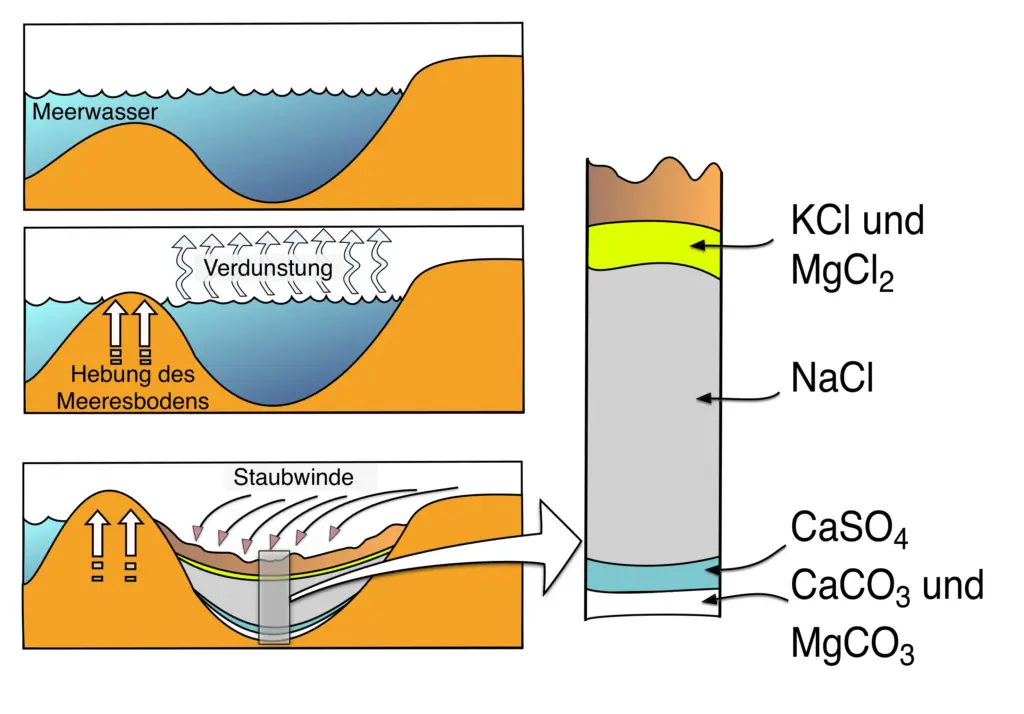
Entstehung von Salzlagerstätten
Entstehung einer Salzlagerstätte1
Kochsalzsynthese aus den Elementen
Weiteres
In vielen Schulbüchern findet man die Aussage, dass man Kochsalz herstellt, in dem man elementares Natrium (Na) mit elementarem Chlor (Cl2) reagieren lässt. Das ist prinzipiell korrekt.
Ein zugegebenermaßen altes Video dazu
Natriumchlorid-Herstellung mit Spritzentechnik2
Weiteres
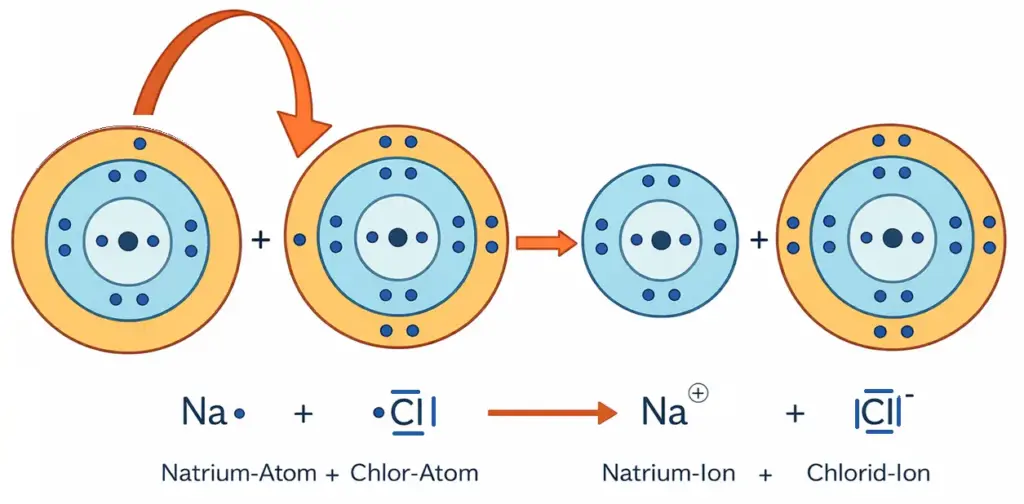
Auf der Teilchenebene findet dabei folgender Vorgang statt:
Prinzipielle Darstellung der Elektronenübertragung im Schalenmodell.3
Weitergedacht
- Erkläre mit Hilfe von M3 was in M2 richtig, aber ungenau dargestellt ist und benenne den energetisch entscheidenden Faktor der Natriumchlorid-Synthese aus den Elementen.
- Suche in M4 nach einem Muster, welche Elemente welche stabilen Ionen bilden.
Genauer hingeschaut
1. Niemand stellt Kochsalz so her!
Wenn du dich an Betrachtung ausgewählter Elementfamilien erinnerst, dann erkennst du, dass dies auf der Erde in den seltensten Fällen geschehen wird:
- Natrium ist ein hochreaktives Metall, das unter einer Schutzflüssigkeit aufbewahrt wird.
- Chlor ist ein sehr aggressives Gas, welches mit vielen Stoffen reagiert.
- Beide Stoffe muss man also eigentlich auf der Erde erst herstellen, denn als Element sind sie an der Luft nicht stabil.
- Ergo: Kochsalz stellt man nur so her, um den „Elektronenübertragungsprozess“ zu zeigen
2. Die Atome "wollen keine Edelgaskonfiguration"
Oftmals findet man dann in den Darstellung Aussagen wie:
„Natriumatome reagieren zu Natrium-Ionen, Chloratome zu Chlorid-Ionen, weil beide ihre Valenzschale füllen wollen. Das ist ein stabiler Zustand.„
Das ist so nicht richtig. Korrekterweise sollte man sagen, dass die Ionisierung meistens bei vollen Schalen aufhört, da man zu einer weitergehenden Ionisierung (Entfernen oder Hinzufügen von Elektronen aus bzw. zu vollen Schalen) viel mehr Energie benötigen würde, als zur Herstellung eines Ions mit voller Valenzschale. Aber: alle Ionisierungsprozesse benötigen Energie.
3. Die Energie stammt aus der Gitterbildung
Daher lässt die Darstellung in Abb. 2 etwas Wichtiges im Nachgang außer acht, was nicht gezeichnet ist.
Die eigentliche Energie stammt aus dem Prozess danach. Du kennst ihn bereits: die Ionen bilden eine stabiles Ionengitter.
Videos und Animationen
Eine alte aber immer noch treffende Darstellung von Ralph-Peter Schmitz und Michael Tausch dazu findest du auf den Seiten der Bergischen Universität Wuppertal.
Dort sind nicht nur gute Videos zum Versuch zu finden, sondern auch eben auch Animationen zum gesamten Prozess auf der Teilchenebene.
Zum Mitnehmen
Weiteres
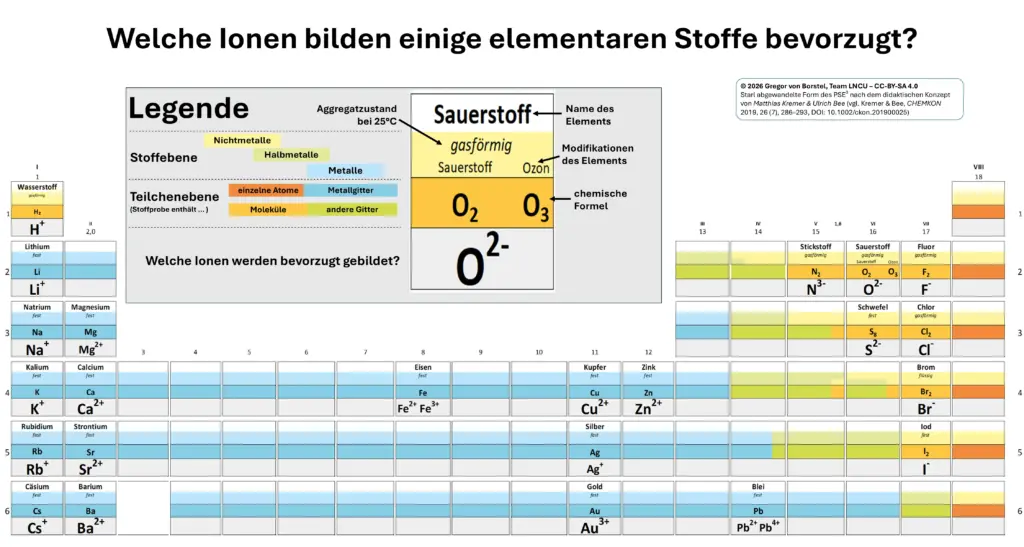
In Abb. 3 siehst du, welche Ionen einige Atome der Elemente bilden. Wir haben aber nicht alle aufgeschrieben!
Von einigen Elementen kennt man keine stabilen Ionen. Andere haben wir hier nicht dargestellt, weil wir sie selten brauchen und wieder andere Elemente bilden gleich mehrere stabile Ionen und sind hier teilweise dann auch nicht dargestellt.
Aber die dargestellten Ionen benötigen wir häufiger. Du kannst die Ansicht immer wieder aufrufen oder auch auswendig lernen. Aber vielleicht erkennst du ja ein Muster?
Weiteres
Exemplarische Auswahl bevorzugt gebildeter Ionen3