Im Gegensatz zum Daniell-Element sind die Zink-Kohle-Batterie oder die Alkali-Mangan-Batterie eine im Alltag gebräuchliche mobile Stromquelle, zum Beispiel in Fernbedienungen für den Fernseher.
Die beiden Batterietypen weisen gemeinsame Baumerkmale, aber auch Unterschiede auf.
Weiteres
Einsatzorte für Batterien.1
Aufgaben
- Bereiten Sie eine Präsentation zu eines der in M1 genannten Batterien vor, indem Sie …
- … den Aufbau und die chemischen Abläufe in der jeweiligen Zelle recherchieren.
- … den jeweiligen fotographischen Querschnitt beschriften.
- … die jeweilige Auswertungshilfe ausfüllen.
- … möglichst viele Abschnitte der jeweiligen Entladekurve unter Verwendung von Gleichgewichtsbetrachtungen bzw. der Nernst-Gleichung erklären.
- Betrachten Sie die Videos in M2 und beurteilen Sie das darin enthaltene Werbeversprechen.
- Erläutern Sie, inwiefern die Alkaline-Batterie eine Weiterentwicklung der Zink-Kohle-Batterie sein könnte.
Material
Alkali-Mangan-Batterien
Querschnitt durch eine Alkali-Mangan-Batterie.1
Entladekurve
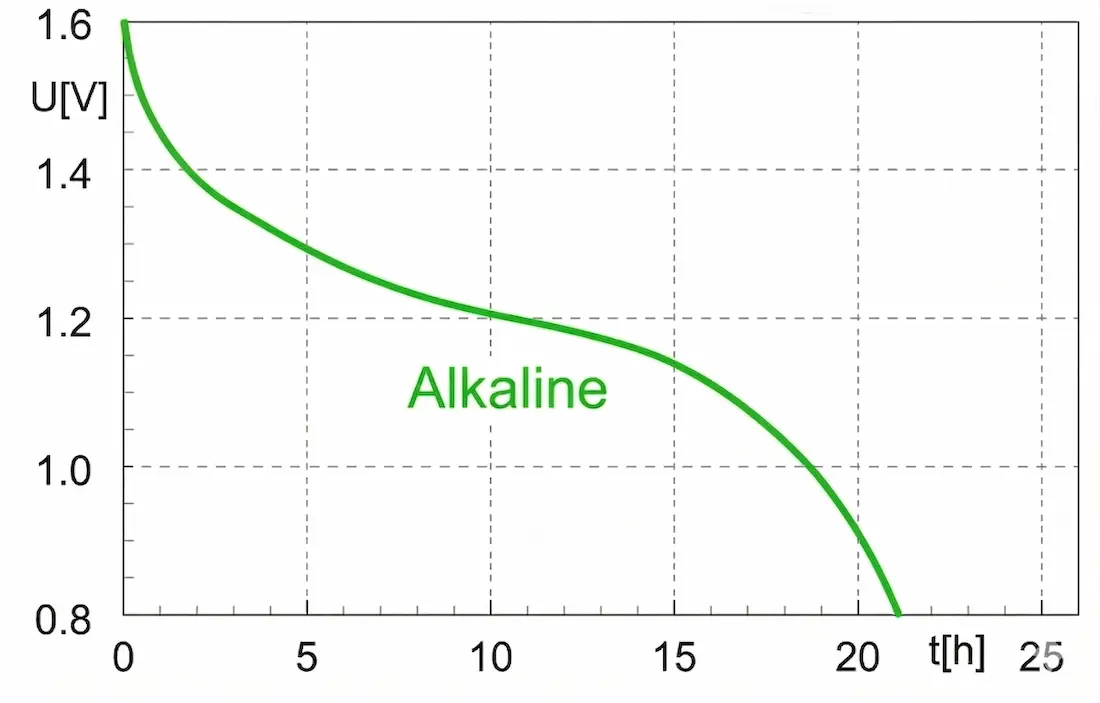
Spannungsverlauf bei der Entladung einer Alkaline-Batterie bei gleicher Größe wie eine Zink-Kohle-Batterie. Konstanter Entladestrom von 120 mA.2
Anregungen
Im Vergleich zur Entladekurve einer Zink-Kohle-Batterie zeigt diese Entladekurve einen weniger steilen Abstieg. Warum ist das so?
- Als Anode liegt hier Zink in Pulverform vor. Dadurch ist seine Oberfläche sehr groß, sodass die Bildung von Zink-Ionen erleichtert ist.
- Die Alkaline-Batterie nutzt konzentrierte Kalilauge (KOH) als Elektrolyt, einem sehr guten Ionenleiter. Kalilauge liegt hier vollständig dissoziiert vor. Zudem weisen Hydroxid-Ionen durch den Grotthuss-Mechanismus eine hohe Ionenbeweglichkeit auf. All das senkt den elektrischen Innenwiderstand der Batterie. Die Spannung bleibt auch dann relativ stabil, wenn man viel Strom entnimmt.
- Zu Beginn entsteht lösliches Zinkat [Zn(OH4)]2-. Irgendwann ist der Elektrolyt mit Zinkat gesättigt, dann fällt Zinkoxid (ZnO) als schwerlösliches Salz aus und erhöht den Durchtrittswiderstand für jegliche Ionen im Elektrolyten.
- Durch die Elektrodenreaktionen wird Wasser verbraucht: Der Elektrolyt wird zäher, wodurch jede Diffusion gehemmt wird.
- In einer Nebenreaktion kann an der Anode Wasserstoffgas entstehen: Dieses verschlechtert den Kontakt zwischen Elektrode und Elektrolyt.
Auswertungshilfe
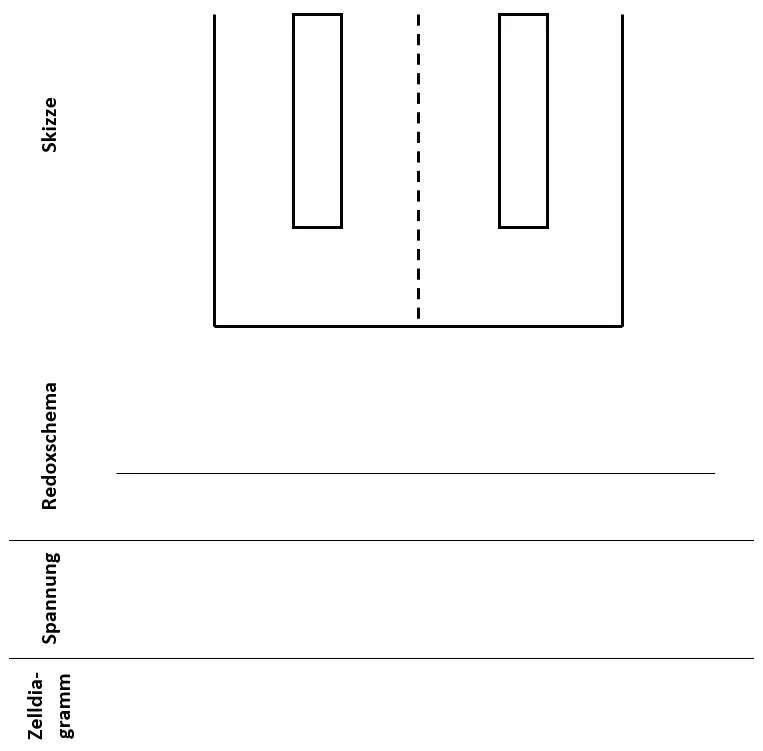
Eine Zink-Kohle-Batterie
Querschnitt durch eine Zink-Kohle-Batterie.1
Entladekurve
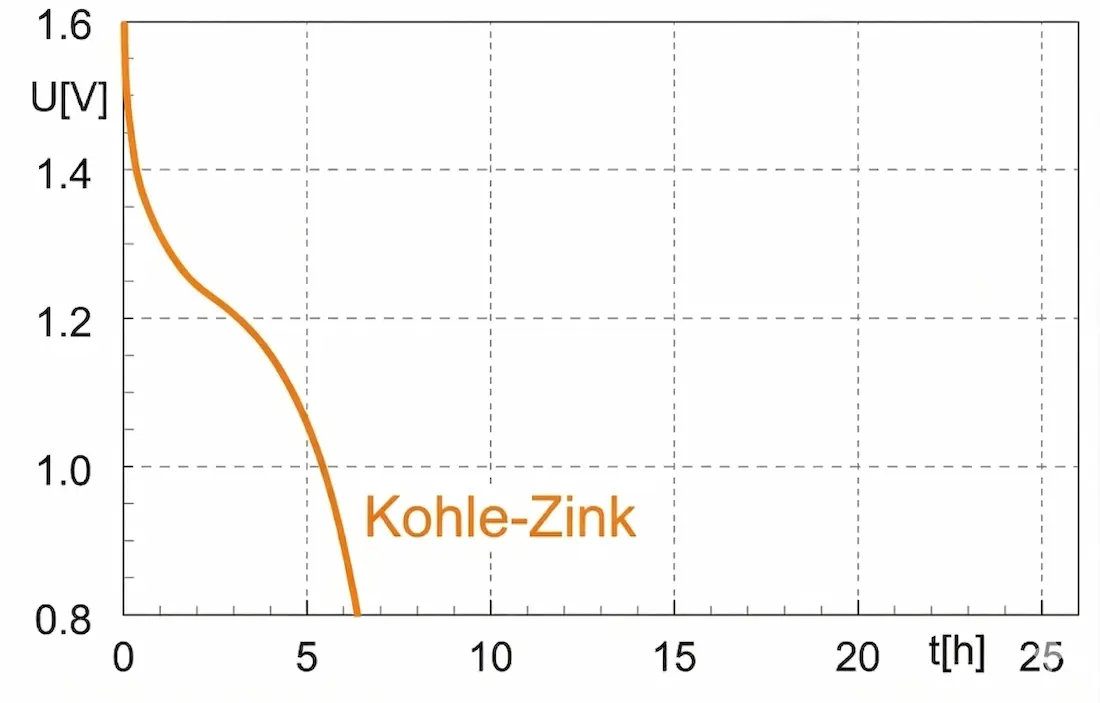
Spannungsverlauf bei der Entladung einer Zink-Kohle-Batterie bei gleicher Größe wie eine Alkaline-Batterie. Konstanter Entladestrom von 120 mA.2
Anregungen
Im Vergleich zu den Entladekurven der anderen Gerätebatterien zeigt diese Entladekurve einen stetigen und steilen Abstieg. Warum ist das so?
- Die Anode ist ein Zinkbecher. Die Reaktion findet nur an der Innenseite des Bechers statt (geringe Oberfläche). Sobald die Innenseite von Zink-Ionen oder anderen Reaktionsprodukten belegt ist, bricht die Leistung ein. Damit die Reaktion weitergeht, müssen diese von der Zinkoberfläche wegwandern.
- Der Elektrolyt Ammoniumchlorid (NH4Cl) ist mit Stärke oder Mehl angedickt, um eine feste Paste zu erzeugen. Die Diffusionsgeschwindigkeit jeglicher Ionen ist hier gering.
- An der Kathode entsteht Ammoniak (NH3). Dieses bildet mit Zink- und Chlorid-Ionen aus dem Elektrolyten ein schwerlösliches Salz: Diamminzinkchlorid [Zn(NH3)2]Cl2. Dieses fällt aus und bildet eine Art Kruste direkt an der Zinkelektrode. Neue Zink-Ionen müssen durch diese Kruste hindurchdiffundieren.
- Wenn der Abtransport an Zink-Ionen so langsam erfolgt, entsteht an der Zink-Oberfläche eine sehr hohe Konzentration von Ihnen. Gemäß der Nernst-Gleichung wird dadurch das Potential der Anode positiver. Die Gesamtspannung sinkt.
Auswertungshilfe

NiMH- und Lithium-Ionen-Akkus
Querschnitt durch eine Rundzelle mit Sandwich-Struktur (Jelly Roll).1
Entladekurve
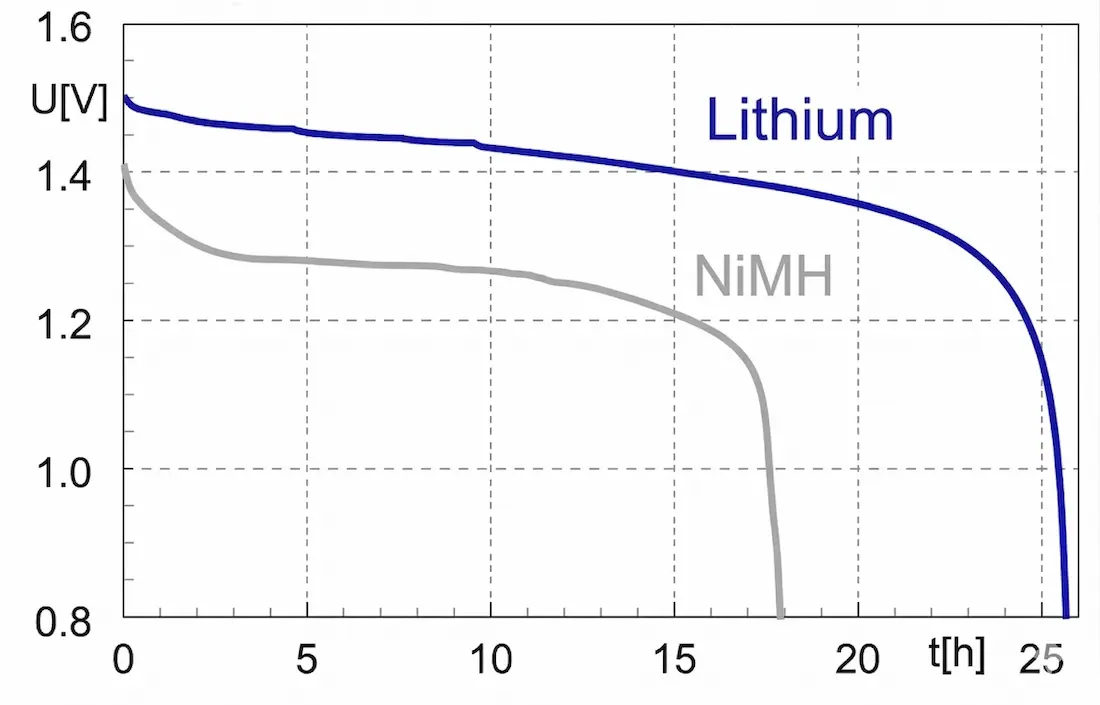
Spannungsverlauf bei der Entladung eines NiMH- und Lithium-Ionen-Akkus bei gleicher Größe wie eine Alkaline oder Zink-Kohle-Batterie. Konstanter Entladestrom von 120 mA.2
Anregungen
Im Vergleich zur Entladekurve einer Zink-Kohle-Batterie zeigen diese Entladekurven ein breites Plateau, gefolgt von einem steilen Abfall. Warum ist das so?
- Kein chemischer Umbau der Elektroden: Es gibt ein Wirtsgitter, in das Gast-Ionen hineinschlüpfen. So lange Plätze frei sind, ändert sich das chemische Potential der Elektrode kaum. Das Potential knickt erst ein, wenn die letzten freien Plätze besetzt werden und die Ionen beginnen, sich gegenseitig abzustoßen.
- Der Innenwiderstand bleibt stabil, da keine isolierenden Krusten auf den Elektroden wachsen.
Auswertungshilfe

Akkuanzeige in Smartphones
Die Prozentanzeige für den Akku deines Smartphones ist größstenteils das Ergebnis eines Algorithmus, nicht einer direkten Messung einer „Füllmenge“.
- Erklären Sie, warum es für die Software viel schwieriger ist, den Unterschied zwischen 80 % und 75 % zu berechnen als den Unterschied zwischen 10 % und 5 %.
- Programmieren Hersteller ihrer Meinung nach die Software so, dass das Smartphone bei 100 % gefühlt ewig hält, aber bei 5 % rast? Ist das Täuschung oder unvermeidbar?
Anregungen
- Im Bereich von 80 % bis 75 %: Die Spannung sinkt hier nur extrem minimal ab (oft nur um wenige Millivolt, z. B. von 3,85 auf 3,80 V. Da Sensoren immer eine gewisse Messungenauigkeit haben, kann die Software allein anhand der Spannung kaum unterscheiden, ob der Akku bei 78 % oder 72 % steht. Ein kleiner Laststoß (z. B. das Display wird kurz heller) lässt die Spannung stärker schwanken, als es die Entladung selbst tun würde.
- Technisch gesehen wird ein Akku selten bis zum absoluten chemischen Maximum geladen, um die Lebensdauer zu schonen. Die Software deklariert diesen „sicheren Maximalzustand“ einfach als 100 %.
- Im Bereich von 10 % bis 5 %: Hier befindet sich der Akku in der „Absturzphase“. Die Spannung sinkt pro entnommener Ladungseinheit sehr stark (steil abfallende Kurve). Eine Differenz von 5 % Kapazität entspricht hier einem deutlichen Spannungsabfall (z. B. von 3,4 auf 3,1 V). Dieser große Unterschied ist für die Sensoren sehr leicht und präzise messbar.
- Fazit: Im Plateau-Bereich muss die Software „blind“ die ausgeflossenen Ladungsträger zählen (Coulomb Counting), was fehleranfällig ist. Am Ende liefert die Spannung eine klare, aber leider auch sehr „kurzfristige“ Information.
- Da der Innenwiderstand eines fast leeren Akkus ansteigt, sorgt jede Aktion (z. B. eine Nachricht senden) für einen massiven, kurzzeitigen Spannungseinbruch. Die Software registriert diesen Einbruch und korrigiert die Prozentanzeige hektisch nach unten, um eine plötzliche Abschaltung zu verhindern.
- Die Anzeige „0 %“ ist eine Schutzlüge. Chemisch gesehen ist der Akku dann noch nicht völlig leer, aber die Software schaltet das Gerät ab, um die Chemie vor irreversiblen Schäden durch Tiefentladung zu schützen. Da dieser Sicherheitsbereich unantastbar ist, bleibt für die „echte“ Nutzung am Ende weniger Zeit, als die Prozentzahl suggeriert.
Energie- und Kosteneffizienz
- Nennen Sie mögliche Gründe, für die Tatsache, dass weltweit weiterhin Zink-Kohle- und Alkaline-Batterien hergestellt und verkauft werden. Nutzen Sie hierfür die Abb. 8 Abb. 9 und Abb. 10 in M3.
- Vollziehen Sie die Rechnung in M3 nach.
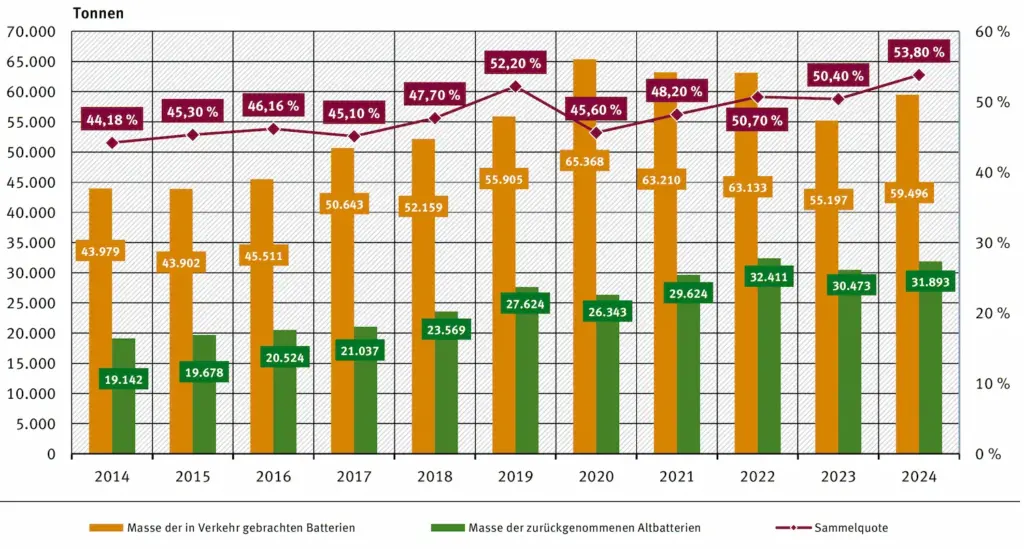
- Beurteilen Sie basierend auf Abb. 7, ob es sich bei der Sammelquote um einen Erfolg oder Misserfolg handelt.
- Benennen Sie Möglichkeiten, die Sammelquote in Deutschland zu steigern.
Verpackte Energie zu welchem Preis?
Weiteres
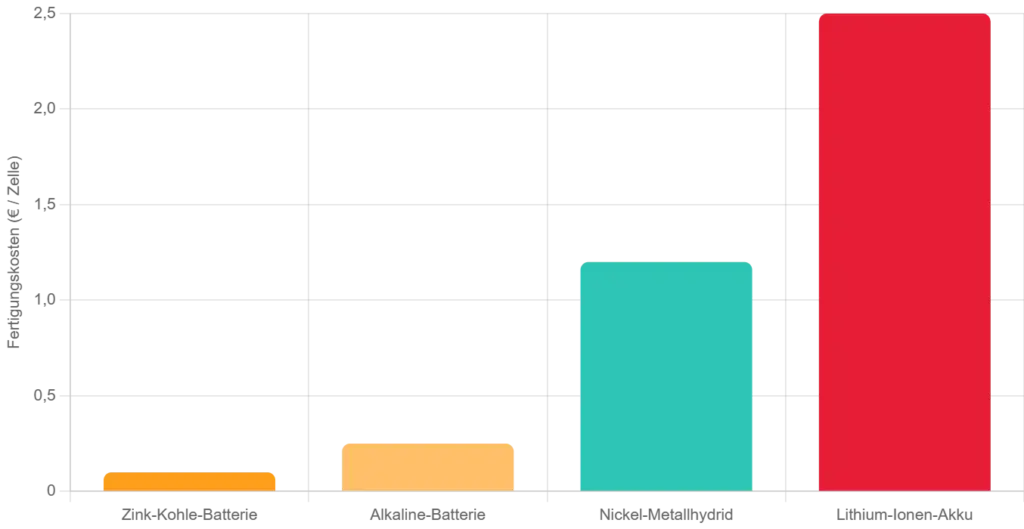
Herstellungskosten pro Zelle im Vergleich.5
Anregungen
Dieses Balkendiagramm verdeutlicht die massiven Unterschiede in den initialen Produktionskosten. Lithium-Ionen-Zellen sind in der Herstellung bis zu 25-mal teurer als einfache Zink-Kohle-Batterien. Dies liegt an teuren Rohstoffen (Lithium, Kobalt) und anspruchsvollen Produktionsbedingungen (Reinräume).
Weiteres
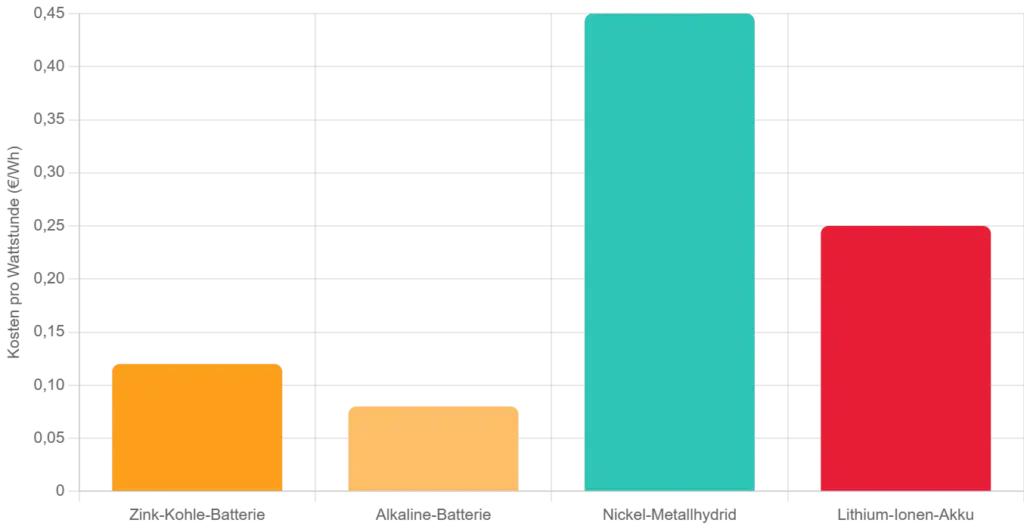
Kosten pro Wattstunde (Wh) im Vergleich. 5
Anregungen
Betrachtet man die Kosten pro Wattstunde (Wh), verschiebt sich das Bild. Alkaline bietet bei Primärzellen das beste Verhältnis. Lithium-Ionen sind zwar initial teuer, bieten aber extrem hohe Energiedichten, was die höheren Kosten pro Wh in mobilen High-End-Anwendungen rechtfertigt.
Weiteres
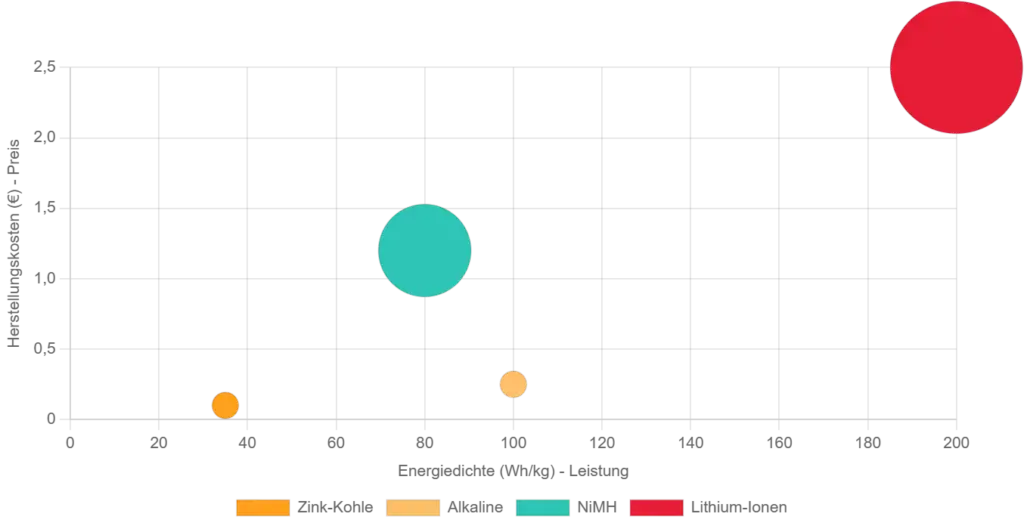
Blasendiagramm. Größe der Blase = Zyklenfestigkeit.5
Anregungen
Dieses Blasendiagramm visualisiert das komplexe Zusammenspiel der drei wichtigsten Faktoren: Die X-Achse zeigt die Energiedichte (Leistungsgewicht), die Y-Achse die Herstellungskosten. Die Größe der Blase repräsentiert die Zyklenfestigkeit (Lebensdauer). Es wird klar: Höhere Kosten erkaufen signifikant mehr Leistung und Wiederverwendbarkeit.
Energie aus Batterien ist mindestens 200-mal teurer, als Energie aus der Steckdose.
Energie- & Kosteneffizienz
„Batterien (nicht wiederaufladbar) und Akkus (wiederaufladbar) liefern – „jenseits der Steckdose“ – Strom für mobile Anwendungen. Nicht wiederaufladbare Batterien tun dies allerdings auf sehr ineffiziente Art und Weise. Denn Batterien benötigen für ihre eigene Herstellung 40- bis 500-mal mehr Energie, als sie bei der Nutzung später zur Verfügung stellen. Ähnlich ungünstig sieht es mit den Kosten aus.
Eine Beispielrechnung zeigt dies sehr eindrucksvoll: Aktuell müssen Verbraucher*innen ca. 0,35 € für eine Kilowattstunde (kWh) elektrische Energie aus der Steckdose zahlen. Möchte man die gleiche Energiemenge (1 kWh) durch Batterien bereitstellen, z.B. mit AA-Batterien, müssten hingegen rund 80 € ausgegeben werden (AA-Batterie: 2.600 mAh * 1,5 V = 0,0039 kWh/Batterie, ca. 0,32 €/Stück). Vereinfacht bedeutet das: Energie aus Batterien ist mindestens 200-mal teurer, als Energie aus der Steckdose. Noch ungünstiger fällt der Vergleich aus, wenn die kleineren AAA-Batterien eingesetzt werden (AAA-Batterie: 1.250 mAh * 1,5 V = 0,0019 kWh/Batterie, ca. 0,40 €/Stück): Hier müssen ca. 200 € ausgegeben werden, um 1 kWh elektrische Energie aus der Steckdose zu ersetzen bzw. ca. 500-mal mehr, als für Strom aus der Steckdose.“6