Gedanken vorab
Weiteres
Bevor ich den Plan für den Unterrichtsbesuch schreibe, habe ich Folgendes schon fertig durchdacht.
Die Stellung der Stunde in der Reihe
Die Stunde ist am Ende der Bindungsreihe angesiedelt und bündelt zentrale zuvor erarbeitete Konzepte wie Ionengitter, Wasser als Dipol sowie Ionen-Dipol-Wechselwirkungen im Modell des Lösevorgangs. Aufbauend auf den zuvor experimentell beobachteten Temperaturänderungen beim Lösen verschiedener Salze steht nun die energetische Erklärung dieser Phänomene im Mittelpunkt, bevor in der folgenden Stunde eine systematischere Bewertung der Anwendungen (z. B. Hotpots und Kühlpacks) erfolgt.
Was genau will ich heute unterrichten?
„Warum wird ein Hotpot heiß? – Energetische Betrachtung des Lösevorgangs von Salzen auf Teilchenebene und erste Beurteilung der Sinnhaftigkeit selbsterhitzender Instant-Lebensmittel.“
Im Zentrum der Stunde steht die modellhafte Erklärung von Temperaturänderungen beim Lösen von Salzen durch die energetische Gegenüberstellung von Gitterenergie und Hydratationsenergie auf Teilchenebene mit einem Fokus auf die leichter zu erklärende Erwärmung im Kontext des Hotpots.
Wie sieht das ideale Lernprodukt aus?
Gedanken zum Lernprodukt1
Lernprogression von den Lernenden aus gedacht
Die Lernenden wissen aus Experimenten, dass sich Lösungen beim Lösen von Salzen erwärmen oder abkühlen können → sie sollen das erklären → dazu betrachten wir den Lösevorgang noch einmal allgemein auf Teilchenebene und überlegen, an welchen Stellen dabei Energie benötigt oder frei wird → die Lernenden benötigen die Begriffe Gitterenergie und Hydratationsenergie → mit einem erweiterten Modell können sie schließlich allgemein erklären, warum Lösungen warm, kalt oder kaum verändert werden und dies auf die Beispiele übertragen.
Welche Materialien nutzen wir?
- Whiteboards und Stifte zur Visualisierung der Filmleisten
- Magnetische Modellmaterialien (Kationen und Anionen) zur Darstellung von Ionengitter und Hydratation
- Bilder sowie reale Produkte (z. B. Hotpot bzw. Kühlkompresse) zur Kontextualisierung des Phänomens
- Digitale Vorlage zur Erstellung einer Filmleiste (drei Bilder)
- Informationstexte zu Hydratationsenergie und Gitterenergie
- Arbeitsaufträge zur schrittweisen Modellierung des Lösevorgangs
- Qualitative Energiediagramme zur Zuordnung verschiedener Lösevorgänge (exotherm, endotherm, nahezu neutral)
Weiteres
Nun notiere ich die Planung derart, dass Andere Schritt für Schritt meine Entscheidungen nachvollziehen können.
Übung
Für ein und die selbe Stunde wurde die Planung nun teilweise in zwei Varianten notiert und in einer Synopse gegenübergestellt. Die Materialien zur Stunde finden Sie unter Warum wird ein Hotpot heiß?
- Gehen Sie die Darstellung (EA oder PA) vergleichend durch und stellen Sie begründet heraus ob und an welcher Stelle Ihnen eine der beiden Varianten eher zusagt.
- Benennen Sie Möglichkeiten, die von Ihnen bevorzugte Variante noch zu optimieren (präzisieren, Redundanzen vermeiden, korrigieren, …).
- Reflektieren Sie abschließend, welche Erkenntnisse Sie aus dieser Übung mitnehmen können.
Der Plan einer Stunde - teilweise in zwei Varianten
Thema, Lernziele und konkrete Kompetenzerwartungen
Thema der Unterrichtsstunde
Warum wird ein Hotpot heiß? – Energetische Betrachtung des Lösevorgangs von Salzen auf Teilchenebene und erste Beurteilung der Sinnhaftigkeit selbsterhitzender Instant-Lebensmittel.
Lernziel
Die Schülerinnen und Schüler erklären, warum sich Lösungen beim Lösen bestimmter Salze erwärmen oder abkühlen, indem sie den Lösevorgang auf Teilchenebene als Zusammenspiel von Gitterenergie und Hydratationsenergie modellhaft beschreiben und diesen Energieumsatz zur Erklärung des Funktionsprinzips eines Hotpots heranziehen.
Konkretisierte Kompetenzerwartungen
- Die Schülerinnen und Schüler beschreiben den Lösevorgang eines Ionenkristalls in Wasser sowohl auf makroskopischer als auch auf submikroskopischer Ebene und verknüpfen ihre Beobachtungen mit einem energetischen Modell des Prozesses.
- Sie erklären, dass beim Lösen eines Salzes Energie zum Aufbrechen des Ionengitters benötigt wird und gleichzeitig Energie bei der Hydratation der Ionen frei wird. Auf dieser Grundlage erläutern sie qualitativ, warum sich Lösungen je nach Salz erwärmen oder abkühlen können.
- Die Lernenden nutzen geeignete Fachbegriffe wie Ionengitter, Hydratation, Gitterenergie und Hydratationsenergie sachgerecht und stellen Zusammenhänge zwischen den Betrachtungsebenen der Chemie her.
- Darüber hinaus wenden sie ihr Modell zur Erklärung des Alltagsphänomens eines selbsterhitzenden Hotpots an und entwickeln erste Überlegungen zur Sinnhaftigkeit solcher Produkte als Grundlage für eine weiterführende Bewertung in der folgenden Unterrichtsstunde.
Curriculare Anbindung und Stellung der Stunde in der Reihe
Die Unterrichtsstunde lässt sich dem Inhaltsfeld 6 „Salze und Ionen“ (IHF 6) des Kernlehrplans Chemie für die Sekundarstufe I zuordnen (vgl. KLP Chemie NRW Sek I, 2019, S. 29–30; Musterschule schulinterner Lehrerplan, 2024), wobei für ein Gelingen Molekülverbindungen und zwischenmolekulare Wechselwirkungen (IHF 8) konform zum schulinternen Lehrplan bereits unterrichtet wurden. So können Ionen in wässriger Lösungen als gegeben und stabil dargestellt (Herdt, 2019), sämtliche Kristallisationsprozesse und Löseprozesse auch auf Teilchenebene thematisiert und anschlussfähiges Fachwissen für die Elektrochemie und die Säure-Base-Chemie als Chemie der wässrigen Lösungen vermittelt werden.
Im Mittelpunkt der Reihe und auch der Stunde steht der Lösevorgang von Salzen. Dabei wird der Kontext selbsterhitzender beziehungsweise selbstkühlender Systeme genutzt, um Struktur-Eigenschafts-Beziehungen von Salzen sowie energetische Aspekte des Lösevorgangs anschaulich zu erschließen und darüber hinaus einen Beurteilungsaspekt mit einzubetten. Dieser „Hotpot-Kontext“ wird in der Literatur als geeigneter problemorientierter Zugang beschrieben, da er Schülerinnen und Schüler dazu anregt, den Zusammenhang zwischen Ionengitter, Hydratation und Lösungswärme zur Erklärung eines alltagsnahen Phänomens zu nutzen (Schütte & von Borstel, 2014).
Die Reihe baut auf der zuvor erarbeiteten Bindungslehre auf und greift zentrale Konzepte wie Ionenbindung, Ionengitter, Wasser als Dipol sowie Ionen-Dipol-Wechselwirkungen auf.
Die Lernenden üben zunächst in Umkehrung der Betrachtung der Kristallbildung aus der Salzlösung eine Darstellung des Lösevorganges auf Teilchenebene, lernen dann die Hotpots und Kühlpacks kennen und führen Experimente zum Lösen verschiedener Salze durch um empirisch festzustellen, dass der Lösevorgang tatsächlich zum Erwärmen oder Abkühlen führen kann. Die hier geplante Stunde dient anschließend dazu, diese Beobachtungen auf Teilchenebene energetisch zu erklären und auf Anwendungen wie Hotpots oder Kühlpacks zu übertragen.
Die energetische Betrachtung der Lösevorgänge ist in der Sekundarstufe I sicherlich fakultativ. Im Zusammenhang mit den betrachteten Kontextenten eröffnet sie aber viele Möglichkeiten bis hin zu einer Bewertung solcher Produkte in der Folgestunde nach dem WAAGE(R)-Modell (Langlet, J., Eilks, I. et. al. 2022, s. hierzu auch Potenzial des Unterrichtsgegenstandes).
Die Materialien der Reihe werden über die Plattform Lebensnaher Chemieunterricht (LNCU) bereitgestellt:
- Der Lösevorgang auf Teilchenebene: Das Salz in der Suppe – Einführung in das Lösen von Salzen
- Kontextualisierung und Experiment: Kennst du schon den Hotpot? – Problemstellung und Kontext
- Stunde der Unterrichtsplanung: Warum wird ein Hotpot heiß? – energetische Betrachtung des Lösevorgangs
- Beurteilung der Produkt: Hotpots und Kühlpacks – sinnvoll oder überflüssig?
- Reflektion der Beurteilung: Ist das gut oder schlecht? – Ein begründetes Urteil fällen
Lehr- und Lernvoraussetzungen
Die Lerngruppe ist eine Regelklasse der Jahrgangsstufe 9. Die 30 Schülerinnen und Schüler sind an experimentelles Arbeiten im Chemieunterricht gewöhnt und verfügen über Erfahrung in der Bearbeitung von Lernaufgaben sowie in kooperativen Arbeitsformen wie Partner- und Gruppenarbeit. Die Arbeit mit Lernmaterialien, die eigenständige Erarbeitung fachlicher Zusammenhänge sowie die anschließende Präsentation und Diskussion von Ergebnissen sind den Lernenden aus dem bisherigen Unterricht vertraut.
Fachlich bauen die Schülerinnen und Schüler auf grundlegenden Kenntnissen aus der Bindungslehre auf. Atombau, Ionenbildung, Ionenbindung und der Aufbau von Ionengittern wurden zuvor behandelt und gesichert. Ebenso wurden Eigenschaften von Salzen sowie Wasser als polares Lösungsmittel thematisiert. Die Hydratation von Ionen wurde bereits eingeführt und mehrfach genutzt, um Lösevorgänge auf Teilchenebene zu beschreiben. Auch energetische Grundvorstellungen zu exothermen und endothermen Prozessen sowie einfache Energiediagramme sind den Lernenden bekannt.
Die Verbindung zwischen makroskopischer Beobachtung, Teilchenebene und symbolischer Darstellung wurde im bisherigen Unterricht wiederholt eingeübt. Insbesondere der Einsatz von Filmleisten zur Modellierung chemischer Vorgänge auf Teilchenebene ist den Schülerinnen und Schülern vertraut und wurde bereits mehrfach erfolgreich genutzt. Dadurch verfügen sie über grundlegende Strategien, um chemische Prozesse modellhaft zu beschreiben und unterschiedliche Betrachtungsebenen miteinander zu verknüpfen.
Die sprachlichen Voraussetzungen der Lerngruppe sind insgesamt homogen, sodass fachsprachliche Begriffe und erklärende Darstellungen im Unterricht in der Regel gut aufgegriffen und weiterentwickelt werden können. Die Schülerinnen und Schüler sind daran gewöhnt, ihre Beobachtungen und Erklärungen unter Verwendung zentraler Fachbegriffe zu formulieren und diese in kooperativen Arbeitsphasen gemeinsam zu diskutieren.
Sachanalyse und didaktische Schwerpunktsetzung
Für die vorliegende Stunde ist der Löseprozess eines Salzes zentral. Beim Lösen eines Salzes in Wasser werden Ionen aus dem Ionengitter gelöst und von Wassermolekülen umgeben (Hydratation).
Dabei wirken zwei energetische Teilprozesse: Zum einen muss Energie aufgewendet werden, um die elektrostatischen Anziehungskräfte im Ionengitter zu überwinden (Gitterenergie), zum anderen wird Energie frei, wenn sich Wassermoleküle an die Ionen anlagern (Hydratationsenergie).
Ob sich eine Lösung beim Lösen eines Salzes erwärmt oder abkühlt, hängt davon ab, welcher Energiebetrag überwiegt. Übersteigt die Hydratationsenergie die Gitterenergie, verläuft der Prozess exotherm; im umgekehrten Fall endotherm.
Die Auswahl der verwendeten Salze für die Unterrichtssequenz orientiert sich an realen Anwendungen. Selbstkühlende Einweg-Kältekissen enthalten häufig phlegmatisierte Stickstoffsalze wie Ammoniumnitrat. In selbsterhitzenden Systemen wird hingegen häufig wasserfreies Calciumchlorid eingesetzt. Beide Beispiele eignen sich daher in besonderer Weise, um energetische Aspekte von Lösevorgängen im Kontext alltagsnaher Anwendungen zu thematisieren (Schütte, P. & von Borstel, G., 2014).
Im Unterricht wird dieser Zusammenhang daher bewusst anhand von Hotpots und Kühlpacks veranschaulicht, denn gleichzeitig eröffnen diese Kontext eine BNE-Perspektive, da die Nutzung solcher Einwegprodukte auch hinsichtlich Ressourcenverbrauch und entstehendem Verpackungsmüll kritisch reflektiert werden kann.
Potenzial des Unterrichtsgegenstandes
Beim Lösen eines Ionenkristalls in Wasser laufen zwei energetische Teilprozesse ab, deren Zusammenspiel die beobachtete Temperaturänderung bestimmt. Zunächst lösen einzelne Ionen aus dem Ionengitter. Dieser Schritt erfordert Energie, da die elektrostatischen Anziehungskräfte zwischen Kationen und Anionen im Kristall überwunden werden müssen. Der damit verbundene Energieaufwand wird durch die Gitterenergie beschrieben.
Beim Lösen werden die Ionen von Wassermolekülen umgeben. Die polaren Wasserdipole richten sich dabei elektrostatisch zu den geladenen Ionen aus. Diese Hydratation ist mit einer Energieabgabe verbunden, die als Hydratationsenergie bezeichnet wird.
Eine zu beobachtende Temperaturänderung ergibt sich aus der Bilanz dieser beiden Energiebeiträge:
- Übersteigt die freiwerdende Hydratationsenergie den Energieaufwand zum Aufbrechen des Ionengitters, wird insgesamt Energie an die Umgebung abgegeben. Der Lösevorgang verläuft exotherm und die Lösung erwärmt sich.
- Ist dagegen der Energiebedarf für die Zerstörung des Ionengitters größer als die bei der Hydratation freiwerdende Energie, muss zusätzliche Energie aus der Umgebung aufgenommen werden. Der Lösevorgang ist dann endotherm, und die Lösung kühlt ab.
Für den Unterricht geeignete, wenig gefährliche und gut beobachtbare Beispiele sind der stark exothermen Lösevorgang Calciumchlorid und der stark endotherme Lösevorgang von Ammoniumnitrat (Wagner, 2021).
Genau diese Auswahl der verwendeten Salze ermöglicht zugleich einen Kontextbezug:
- Selbstkühlende Einweg-Kältekissen enthalten häufig phlegmatisierte Stickstoffsalze wie Ammoniumnitrat.
- In selbsterhitzenden Systemen wird hingegen häufig wasserfreies Calciumchlorid eingesetzt.
Die gewählten Salze eignen sich daher in besonderer Weise, um energetische Aspekte von Lösevorgängen im Kontext alltagsnaher Anwendungen zu thematisieren.
Diese kontextualen Anwendungen erfüllen keinen Selbstzweck. Zum einen lassen sich damit exotherme Anwendungen und endotherme Anwendungen gleichermaßen auf denselben grundlegenden energetischen Mechanismus des Lösevorgangs zurückführen und zum anderen eröffnen sich Beurteilungsmöglichkeiten (Schütte, P. & von Borstel, G., 2014).
Der Unterrichtsgegenstand führt somit zentrale Aspekte der Bindungslehre und eine energetischen Betrachtung des Lösevorgangs zusammen. Er bahnt die qualitative Betrachtung der Lösungsenthalpie in der Sekundarstufe II an und eignet sich in besonderer Weise für anwendungsbezogene und bewertende Fragestellungen.
Didaktische Reduktion
Die energetische Betrachtung des Lösevorgangs wird in der Unterrichtsstunde bewusst auf ein qualitatives Modell reduziert. Quantitative thermodynamische Daten oder exakte Enthalpiewerte werden bewusst nicht behandelt, obwohl entsprechende Messwerte (Wagner, 2021) grundsätzlich verfügbar wären, da diese erst im Rahmen der Löseenthalpie in der Sekundarstufe II betrachtet werden.
Ausgangspunkt der Modellierung bilden die zuvor experimentell untersuchten Salze, die exemplarisch die drei möglichen Beobachtungen beim Lösen eines Salzes abdecken: Erwärmung, nahezu keine Temperaturänderung und Abkühlung der Lösung. Auf dieser Grundlage entwickeln die Schülerinnen und Schüler ein allgemeines Teilchenmodell mit Kationen und Anionen, das alle drei Phänomene erklären kann.
Da selbsterhitzende Getränkebecher (Schütte, P. & von Borstel, G., 2014) als Unterrichtsgegenstand heute nur noch schwer erhältlich sind, dienen in der Sequenz stattdessen leicht verfügbare selbstheizende Instant-Mahlzeiten, etwa asiatische Hot-Pot-Sets, die vielen Lernenden aus sozialen Medien bekannt sind, als ein Anschauungsobjekt. Dass in diesen Produkten die Wärme allerdings durch die Reaktion von Calciumoxid mit Wasser unter Bildung einer alkalischen Lösung erzeugt wird, wird erst in der Folgestunde bei der Bewertung thematisiert. Neben der exothermen Reaktion von Calciumoxid zu Calciumhydroxid trägt in diesen Hot-Pot-Sets zudem auch Reaktion von Aluminium unter Bildung von Wasserstoff und eines Aluminat-Komplexes [Al(OH)4]–, zur Wärmeentwicklung bei. Da die Reaktion deutlich über den in der Stunde betrachteten Lösevorgang hinausgeht und zusätzliche chemische Konzepte erfordern würden, wird sie im Sinne einer didaktischen Elementarisierung nicht erörtert. Die komplexeren Redoxprozesse dieser Reaktion lassen sich später in der Sekundarstufe II im Zusammenhang mit Aspekten der Korrosion wie Passivierung oder Opferanode aufgegreifen (Böhm, A. & von Borstel, G., 2014).
Strukturiererung der Lernprogression aus der Perspektive der Lernenden
Die Lernenden müssen folgende (gedankliche) Schritte durchlaufen:
- Wir haben bereits einen Lösevorgang auf Teilchenebene beschrieben und in Experimenten konnten wir beobachten, dass sich Lösungen beim Lösen verschiedener Salze erwärmen, abkühlen oder kaum eine Temperaturänderung zeigen.
- Im Prozess des Lösevorgang wird Energie benötigt oder freigesetzt, aber was genau können wir zum jetzigen Zeitpunkt nicht korrekt benennen.
- Wir müssen ein allgemeines Teilchenmodell entwickeln, das den Prozess des Lösens mit Kationen und Anionen beschreibt und dieses um eine energetische Perspektive erweitern.
- Im Lösevorgang gibt es konkurrierende Teilprozesse – das Aufbrechen des Ionengitters und die Hydratation der Ionen durch Wasserdipole.
- Liefert oder benötigt ein Teilprozess mehr Energie als der andere, wird es warm oder kalt
- Mid dem Vergleich der Hydratations- und Gitterengie kann ich die Abläufe im Hotpot, in der Kältekompresse oder beim Lösen von Kochsalz erklären
Dies ist eindeutig eine konzeptbildende Unterrichtsstunde nach Oser (2001). Als zentrales Lernprodukt nach Leisen (2018) können die Lernenden den Lösevorgang modellhaft darstellen, die Konkurrenz von Gitterenergie und Hydratationsenergie durch entsprechende Energiepfeile verdeutlicht und ergänzend ein qualitatives Energiediagramm zuordnen, das den energetischen Verlauf des Lösevorgangs darstellt. Auf diese Weise werden Teilchenebene und symbolische Darstellung miteinander verknüpft.
Didaktisch-methodische Entscheidungen
Die Unterrichtsstunde orientiert sich am LNCU-Material „HOTPOT UND KÜHLPACKS: Polare Bindungen, Ionenbindung und energetische Betrachtung des Lösungsvorgangs“ (von Borstel & Böhm, 2017) wurde jedoch durch einen aktuellen Kontext (selbsterhitzender Hotpot/ Ramen) sowie durch die sprachsensible Methode der Filmleiste erweitert (vgl. Leisen, 2003). Die Filmleiste unterstützt die Lernenden dabei, den Lösevorgang schrittweise auf der Teilchenebene zu strukturieren und sprachlich zu beschreiben.
Der Stundenaufbau folgt dem Lehr-Lern-Modell nach Leisen (2018), das den Lernprozess in eine kompetenzorientierte Lernlinie gliedert.
Zunächst kommen die Lernenden im Kontext an, indem Bilder von Hotpots und Kühlpacks präsentiert werden und Vorwissen über das Experiment aus der vorherigen Stunde aktiviert wird. In der anschließenden Gelenkstelle wird die Problemfrage der Stunde („Wie kann es beim Lösen von Salzen kalt oder warm werden?“) formuliert und damit der Fokus auf eine Erklärung auf Teilchenebene gelenkt. In der Erarbeitungsphase erstellen die Schülerinnen und Schüler mithilfe der Filmleiste und bereitgestellter Materialien (Whiteboard und Modelle der Ionen/ Moleküle) ein Lernprodukt, indem sie den Lösevorgang modellhaft darstellen und mit den Begriffen Gitter- und Hydratationsenergie erklären. In der Sicherungsphase präsentieren die Gruppen ihre Modelle auf Whiteboards, vergleichen diese im Plenum und diskutieren insbesondere die Darstellung des zweiten Bildes der Filmleiste. Auf dieser Grundlage wird die Problemfrage der Stunde mündlich beantwortet und die Modelle ggf. fachlich präzisiert. Die Sprinter-Aufgabe ermöglicht optional einen Transfer zum Kontext der Kühlpacks (vgl. Leisen, 2018).
Der abschließende Transfer besteht in einer ersten intuitiven Bewertung der Nutzung von Hotpots und Kühlkissen. Dabei wird das WAAGE(R)-Modell zur strukturierten Urteilsbildung aufgegriffen, wobei in dieser Stunde vor allem der Schritt des Wahrnehmens im Vordergrund steht (vgl. Langlet et al., 2022). Eine vertiefte Bewertung erfolgt in der folgenden Stunde.
Die Unterrichtstunde ist am Lehr-Lern-Modell nach Leisen orientiert und folgt dabei dem Prinzip einer konzeptbildenden Stunde nach Oser (2001). In dieser erfüllt das Bewusstmachen des Vorwissen (Oser) das Ankommen im Lernkontext sowie die Aktivierung des Vorwissens (Leisen). Der Einstieg der Stunde muss daher bewusst durch Bild und reale Gegenstände an die zuvor durchgeführten Experimente anknüpfen.
Aus dieser Rückbesinnung ergibt sich die leitende Problemfrage der Stunde: Wie können wir uns erklären, dass Lösungen warm oder kalt werden?
In der folgenden Gelenkstelle (weder bei Oser noch bei Leisen explizit benannt) wird deutlich, dass noch wesentliche Fachbegriffe zur Erläuterung der energetischen Beobachtungen fehlen. Auf diese Weise wird Lernenden bewusst, dass die Durcharbeitung des Prototypens unter Nutzung der Fachbegriffe mit einer bekannten Methode nun notwendig ist. Damit werden zugleich Zieltransparenz und Prozesstransparenz hergestellt.
Mit der Erstellung des Lernproduktes (Leisen) können die Lernenden unter Verwendung von Informationstexten zur Gitterenergie und Hydratationsenergie den Prototypen durchlaufen.
Eine Anleitung unterstützt die Lernenden beim Aufbau der dreiteiligen Darstellung des Lösevorgangs. Die Aufgaben sind schrittweise aufgebaut und ermöglichen eine strukturierte Annäherung an das Modell; für schneller arbeitende Gruppen steht zusätzlich eine Sprinteraufgabe zur Verfügung, in der der energetische Ablauf beim Kühlpack erklärt werden kann.
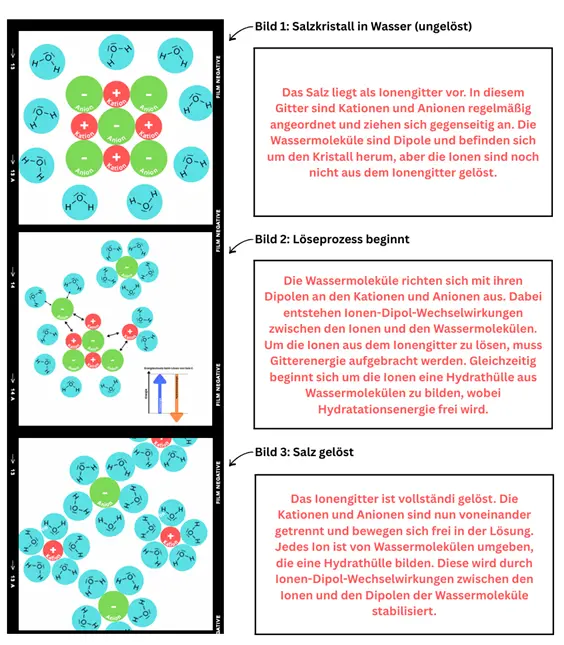
Die Entscheidung für die Arbeit mit Filmleisten dient dazu, den Prozesscharakter des Lösevorgangs für die Schülerinnen und Schüler sichtbar und strukturierbar zu machen. Durch die Darstellung in mehreren aufeinanderfolgenden Bildern wird deutlich, dass es sich beim Lösen eines Salzes nicht um einen punktuellen Vorgang, sondern um einen Prozess handelt, der auf Teilchenebene schrittweise beschrieben werden kann. Insbesondere das mittlere Bild der Filmleiste ermöglicht es den Lernenden, den eigentlichen Übergangszustand des Lösevorgangs zu modellieren und dort konkurrierende energetische Beiträge sichtbar zu machen. Auf diese Weise wird die Aufmerksamkeit gezielt auf den zentralen Erklärungsschritt der Stunde gelenkt.
Zugleich unterstützt die Filmleiste den Wechsel zwischen den Betrachtungsebenen der Chemie. Während die Lernenden auf makroskopischer Ebene bereits Temperaturänderungen beobachtet haben, zwingt die Modellierung auf Teilchenebene dazu, die zugrunde liegenden Prozesse zwischen Ionen und Wasserdipolen darzustellen.
Im Zentrum der Präsentationsphase (Diskussion des Lernprodukts nach Leisen, Beschreiben der wichtigen Merkmale des neuen Konzepts und aktiver Umgang mit dem Konzept nach Oser) stehen das mittlere Bild der Filmleiste, da hier der energetische Kern des Modells sichtbar wird sowie drei Energiediagramme mit unterschiedlichen energetischen Verläufen mit Bezug auf die Kontexte.
Durch die ergänzende Zuordnung von Energiediagrammen wird zusätzlich eine symbolische Darstellungsebene einbezogen. Die Methode unterstützt somit die Verknüpfung makroskopischer Beobachtungen, submikroskopischer Modellvorstellungen und symbolischer Darstellungen und erleichtert den Lernenden den Aufbau eines zusammenhängenden Erklärungsmodells.
Hier fungiert die Filmleiste nun als sprachliches und fachliches Gerüst. Die Schülerinnen und Schüler nutzen gezielt neu eingeführte Fachbegriffe wie Gitterenergie, Hydratationsenergie und Ionen-Dipol-Wechselwirkung, um ihre Darstellung zu beschreiben und zu erläutern.
Die Sicherung (Leisen) kann durch die gemeinsame Zusammenführung der erarbeiteten Modelle erfolgen. Dabei kann das entwickelte Erklärungsmodell vernetzend auf unterschiedliche Fälle (Aktiver Umgang mit dem neuen Konzept nach Oser) angewendet werden, etwa auf Kühlpacks oder auf Natriumchlorid als Beispiel ohne deutliche Temperaturänderung. Auf diese Weise wird deutlich, dass sich alle drei beobachteten Phänomene mithilfe desselben energetischen Modells erklären lassen.
Eine weitere Vernetzung ist mit Blick auf eine Bewertung möglich. Die Schülerinnen und Schüler können abschließend erste spontane Einschätzungen zur Sinnhaftigkeit solcher Produkte zu formulieren, etwa im Spannungsfeld zwischen praktischer Anwendung und ökologischen Fragen wie Verpackungsaufwand oder Ressourcenverbrauch. Diese noch unsystematischen Positionierungen bilden den Ausgangspunkt für die kommende Stunde.
Antizipation von Schwierigkeiten und Diagnosemethoden
Zur Differenzierung werden mehrere Maßnahmen eingesetzt. Während der Gruppenarbeit unterstützen sich die Lernenden gegenseitig, zusätzlich stehen Hilfekarten zur Verfügung , die den Modellbildungsprozess strukturieren. Leistungsstärkere Schülerinnen und Schüler können eine Sprinter-Aufgabe bearbeiten, in der sie ihr Wissen auf den Kontext der Kühlpacks übertragen. Diese Maßnahmen ermöglichen es, unterschiedliche Lernvoraussetzungen innerhalb der Lerngruppe zu berücksichtigen
Eine typische Schwierigkeit besteht darin, dass Schülerinnen und Schüler zwar eine Erwärmung der Lösung plausibel erklären können, jedoch Schwierigkeiten haben, eine Abkühlung des Systems angemessen zu deuten. Häufig wird angenommen, dass Energie beim Lösen grundsätzlich „entsteht“, während der Fall eines endothermen Lösevorgangs schwerer verständlich ist. Insbesondere die Vorstellung, dass für bestimmte Lösevorgänge mehr Energie benötigt wird, als durch die Hydratation frei wird und dass diese zusätzliche Energie aus der Umgebung aufgenommen wird, stellt für viele Lernende eine Herausforderung dar. Da weiterführende Konzepte wie Entropie in dieser Jahrgangsstufe noch nicht behandelt werden, bleibt die Erklärung bewusst auf eine qualitative energetische Betrachtung beschränkt.
Eine weitere mögliche Schwierigkeit besteht in der begrifflichen Unterscheidung zwischen exothermen und exergonischen Prozessen. Ohne gezielte Klärung können diese Begriffe von den Schülerinnen und Schülern vermischt werden, da beide mit Energieabgabe assoziiert werden. In der vorliegenden Stunde wird daher konsequent mit der Vorstellung von Energieaufnahme und Energieabgabe gearbeitet und auf eine präzise Verwendung der eingeführten Begriffe geachtet.
Die Diagnose des Lernstands erfolgt während der Arbeitsphase vor allem über die Analyse der erstellten Filmleisten. Besonders das zweite Bild liefert Hinweise darauf, ob die Lernenden die konkurrierenden energetischen Beiträge des Lösevorgangs verstanden haben. Auch die Zuordnung der bereitgestellten Energiediagramme zu den verschiedenen Fällen erlaubt Rückschlüsse auf das Verständnis der energetischen Zusammenhänge. In der anschließenden Präsentations- und Diskussionsphase werden diese Modelle gemeinsam betrachtet, miteinander verglichen und gegebenenfalls korrigiert, sodass Missverständnisse sichtbar werden und im Plenum aufgegriffen werden können.
Literatur
Böhm, A. & von Borstel, G. (2014). Heater Meals – eine experimentelle Lernaufgabe zur Korrosion für die Sekundarstufe II. CHEMKON, 21(2), 79–84.
von Borstel, G. & Böhm, A. (2017). HOTPOT UND KÜHLPACKS: Polare Bindungen, Ionenbindung und energetische Betrachtung des Lösungsvorgangs. Abgerufen am 3. März 2026, von https://www.lncu.de/files/coursemanager/contenttext/715/tiny/22_hotpot.pdf
Herdt, C. (2019). Teaching ionic bonding – a plea for introducing the term “ion” before explaining ion formation. CHEMKON, 26(6), 237–249. https://doi.org/10.1002/ckon.201900006
Langlet, J., Eilks, I., Gemballa, S., Heckmann, G., Kunz, A., Lübeck, M., Meisert, A., Menthe, J., Ratzek, J., Wlotzka, P., & Wodzinski, R. (2022). Bewertungskompetenz in den Naturwissenschaften: Denkanstöße, Empfehlungen und Hilfen für den Unterricht und für Aufgaben (MNU Themenreihe Bildungsstandards). Deutscher Verein zur Förderung des mathematischen und naturwissenschaftlichen Unterrichts.
Leisen, J. (2003). Filmleiste: Erprobung von Josef Leisen. In UP (Bde. 1–7, S. BSP) [CD-ROM Methoden-Werkzeuge].
Leisen, J. (2018). Was Lehrkräfte brauchen – Ein praktikables Lehr-Lern-Modell.
Ministerium für Schule und Bildung des Landes Nordrhein-Westfalen. (2019). [KLP Chemie NRW SEK I] Kernlehrplan für die Sekundarstufe I Gymnasium in Nordrhein-Westfalen.
Ministerium für Schule und Bildung des Landes Nordrhein-Westfalen. (2022). [KLP Chemie NRW SEK II] Kernlehrplan für die Sekundarstufe II Gymnasium in Nordrhein-Westfalen.
Ministerium für Schule und Bildung des Landes Nordrhein-Westfalen [Leitlinie BNE]. (2019). Leitlinie Bildung für nachhaltige Entwicklung. In Schule in NRW: Bd. Nr. 9052.
Oser, F. K., & Baeriswyl, F. J. (2001). Choreographies of teaching: Bridging instruction to learning.
Schütte, P. & von Borstel, G. (2014): Hotpot – Wie funktioniert ein selbsterwärmendes Heißgetränk? Praxis der Naturwissenschaften – Chemie in der Schule, 63(6), 20–23.
Wagner, T. (2021). Calorimetry meets solvation – how to quantify dissolutions in detail. CHEMKON. 29(5). 10.1002/ckon.202000083.