Wie kann man die Reaktionsgeschwindigkeit gut messen?
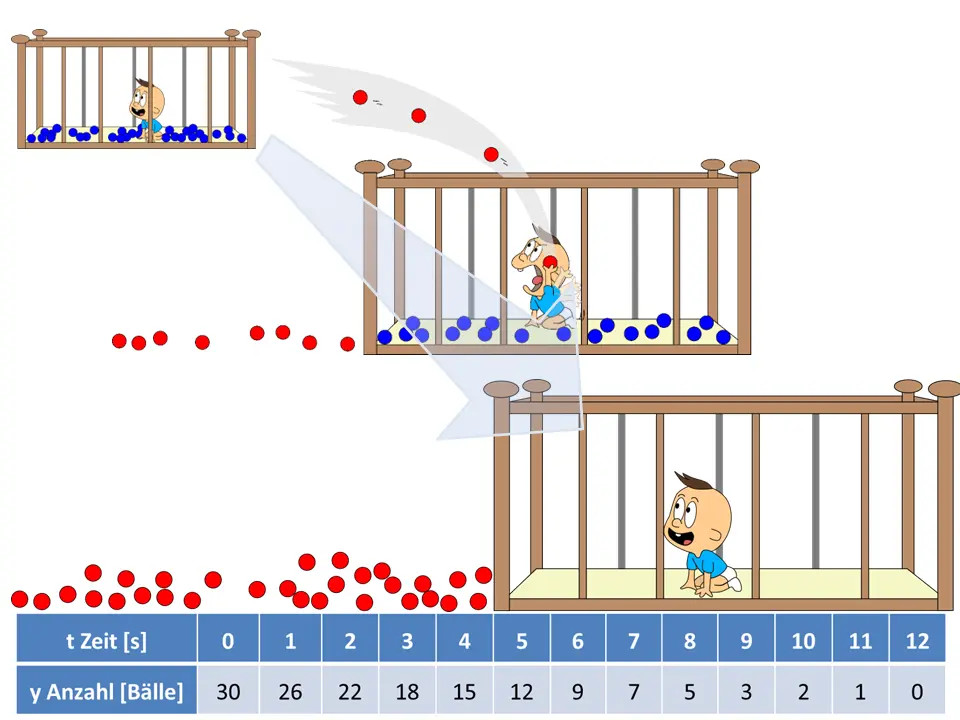
Ich habe jetzt im Bezug auf das Beispiel der Bälle im Kinderzimmer eine Ahnung, dass die Geschwindigkeit dort eine Veränderung der Teilchenzahl in einem Raum pro Zeit bedeutet.
Aber wie ist dies nun bei chemischen Reaktionen?
Die Reaktionsgeschwindigkeit beschreibt eine Veränderung der Teilchenanzahl der Ausgangsstoffe (Edukte) oder der Endstoffe (Produkte) pro Zeitintervall.
Anders als die Bälle im Kinderzimmer kann man Atome oder Moleküle nur sehr schwer einzeln zählen. In Versuchen muss man etwas messen, aus dem man auf die Veränderung der Teilchenzahlen schließen kann.
Aufgaben
- Machen Sie Vorschläge, welche Messgrößen man bestimmen kann, um die Reaktionsgeschwindigkeit zu erfassen.
- Versetzen Sie sich in die Lage, die Reaktionsgeschwindigkeit der Reaktion von Salzsäure mit Magnesium selbst zu ermitteln, indem Sie die Anleitung V1 lesen und ggf. das Zeitraffer-Video betrachten.
- Führen Sie diesen Versuch selbst durch und filmen Sie das Experiment dabei, um es nachfolgend auszuwerten.
Die Geschwindigkeit einer Reaktion messen
Materialien
- Schutzbrille
- 12 mL Spritze
- 30 mL Spritze
- Verbinder luer-lock w-w
- Rückschlagventil luer-lock
- alternativ 3-Wegehahn zum Verschließen
- Becherglas
- Klammer mit Magnet
- fakultativ zum Fixieren während der Filmaufnahme
Chemikalien
-
Salzsäure 1 mol/L
- aus dem Becherglas in die kleine Spritze aufziehen
-
Magnesiumband
- gefaltet ca. 2 cm
Sicherheitshinweis
Es entsteht Wasserstoff: Von Zündquellen fernhalten!
Entsorgen und Aufräumen
-
Alle verunreinigte Labormaterialien spülen.
-
Alle Materialien an ihren Ursprungsort zurückstellen.
-
Restliche Lösung in den Ausguss geben und mit Wasser nachspülen. Entstandenen Wasserstoff im Abzug oder am offenen Fenster in die Luft entlassen.
Durchführung und Aufbau
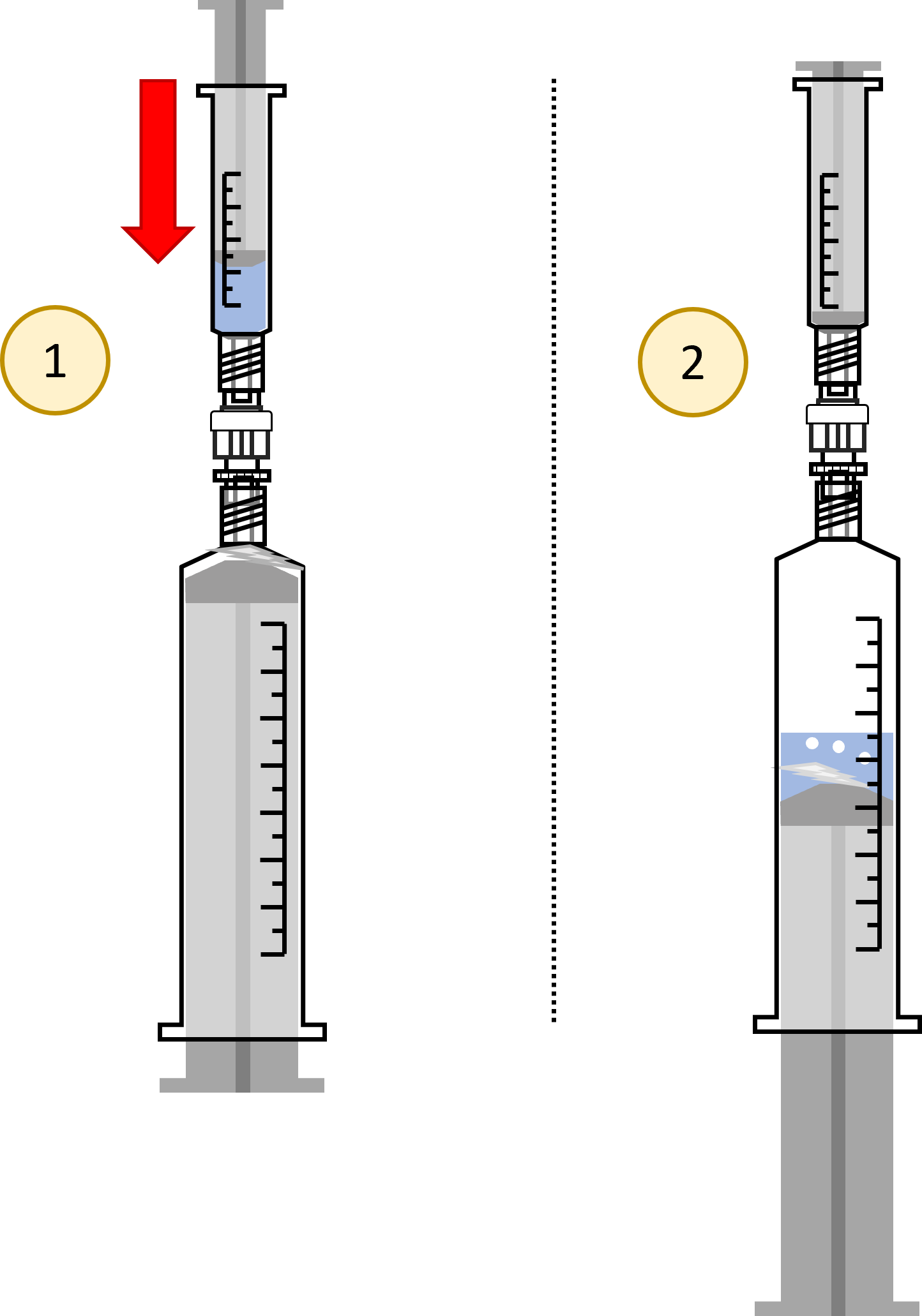
- Die kleine Spritze blasenfrei mit 3 mL Salzsäure befüllen.
- Das Magnesiumband abmessen und in die 30 mL Spritze geben. Die Luft herausdrücken.
- Die große und die kleine Spritze über ein Rückschlagventil und einem Verbinder derart verbinden, dass die Säure zum Magnesium gedrückt werden kann, entstehendes Gas aber nicht entweichen kann. (Pfeilrichtung am Ventil beachten, ggf. vorher ohne Chemikalien testen).
- Die Konstruktion mit einem Magnethalter aufhängen. Der Stempel der 30 mL soll nach unten zeigen! So kann das Volumen leichter abgelesen werden.
- Den Versuch zur besseren Auswertbarkeit filmen! Die Videoaufnahme starten und die gesamte Säure zügig zum Magnesium drücken. Die chemische Reaktion / den Aufbau für ca. 4 Minuten filmen.
Hilfen
Hilfe bei der Auswertung.3
Aufgaben nach der Durchführung des Versuchs
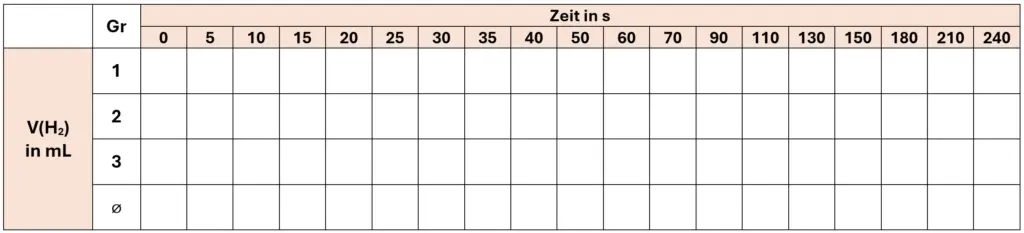
- Legen Sie eine Wertetabelle für den Versuch nach dem Vorbild von Tab. 1 an. Lesen Sie aus Ihrem Video die entsprechenden Werte aus und notieren Sie diese. TIPP: Erkennt man den Flüssigkeitspegel schlecht, kann man stattdessen das Volumen am Stand des schwarzen Gummirings unten am Stempel ablesen und 6 mL davon abziehen.
- Fakultativ: Da die Stempel der Spritzen mitunter schwergängig sind, kann es die Genauigkeit erhöhen, sich von einer oder mehreren Gruppen deren Messwerte geben zu lassen und Durchschnittswerte zu berechnen.
- Reflektieren Sie: Welche Geschwindigkeit können Sie aus den Messdaten ermitteln? Wie ist die Einheit der von Ihnen gemessenen Geschwindigkeit?
- Erstellen Sie aus den Messwerten ein Volumen (V) – Zeit (t) – Diagramm in M2, in welchem Sie die Entstehung des Wasserstoffs (V(H2) in mL) mit der Zeit (t in s) darstellen.
Einen Graphen zeichnen
Weiteres
Weitergehende Übungen
- Bestimmen Sie sowohl aus der Wertetabelle, als auch aus Ihrem Diagramm die Durchschnittsgeschwindigkeit der Bildung von Wasserstoff für ein beliebiges Zeitintervall.
- Versuchen Sie möglichst genau die Anfangsgeschwindigkeit zu bestimmen und vergleichen Sie diese mit der ermittelten Durchschnittsgeschwindigkeit.