Aufgaben
- Begründen Sie mit Hilfe von Abb. 1 und M1 fachsprachlich korrekt, warum die Konzentration der Ionen in den Lösungen einer galvanischen Zelle einen Einfluss auf das Elektrodenpotential hat.
Konzentrationsabhängigkeit des Elektrodenpotentials
Weiteres
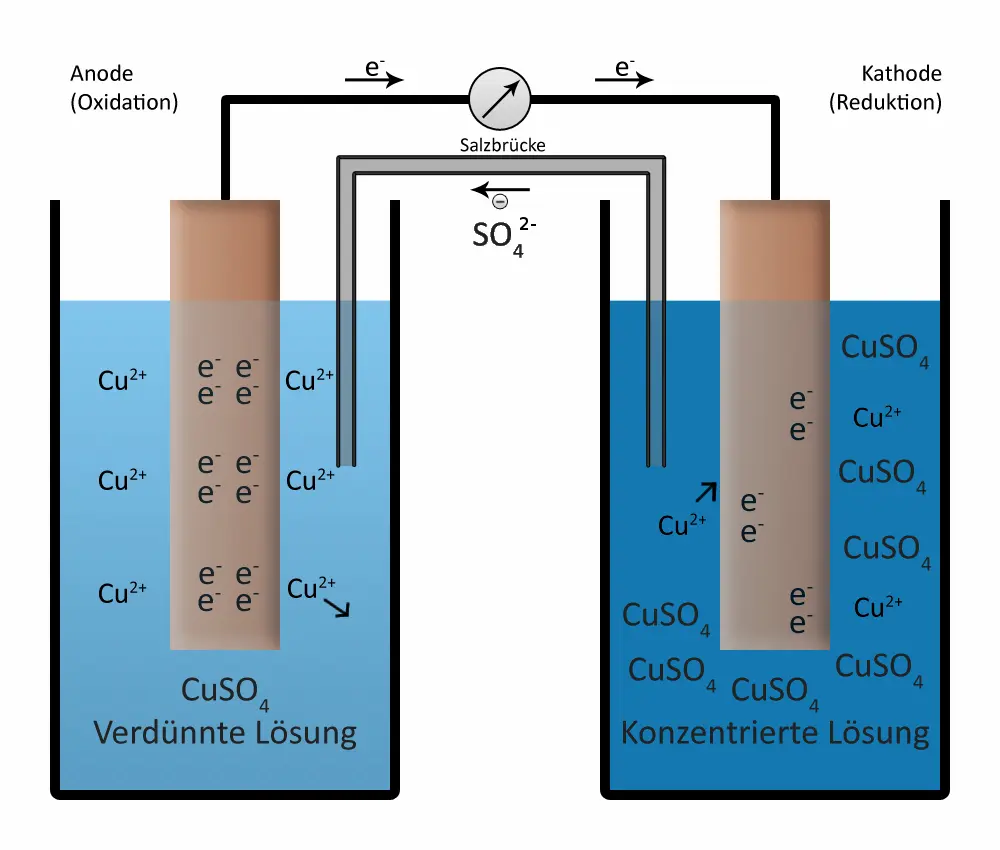
Schematische Darstellung einer Konzentrationszelle am Beispiel des Redoxpaares Cu/Cu2+).1
Kombiniert man zwei Kupfer-Halbzellen mit gleicher Konzentration an Kupfer-Ionen, so ist keine Spannung messbar. Verdünnt man jedoch die Lösung in einer der Halbzellen, so kann man eine Spannung messen. Das gilt beispielsweise für die folgende Kombination:
Galvanische Zellen, die aus Halbzellen des gleichen Redoxpaares mit unterschiedlichen Ionen-Konzentrationen aufgebaut sind, bezeichnet man allgemein als Konzentrationszellen.
Welche Halbzelle bei Konzentrationszellen das niedrigere Elektrodenpotenzial aufweist, lässt sich folgendermaßen erklären: Bis zur Einstellung des elektrochemischen Gleichgewichts müssen in der verdünnteren Lösung mehr Ionen aus dem Metall in Lösung gehen als in der konzentrierteren Lösung. Der Lösungsdruck des Metalls ist in dieser Halbzelle also größer als der Abscheidungsdruck. Damit verstärkt sich die negative Ladung des Metalls. Anders ausgedrückt: Aus der Kupferelektrode treten umso mehr Kupfer-Ionen in die Lösung über, je niedriger ihre Konzentration in der Lösung ist. Diese Elektrode lädt sich stärker negativ auf als die Elektrode in der konzentrierteren Lösung. Damit ist das Elektrodenpotential dieser Halbzelle also niedriger im Vergleich zur Halbzelle mit der höheren Ionenkonzentration. In der Halbzelle, die eine konzentriertere Elektrolyt-Lösung aufweist, findet dementsprechend gegenteiliges statt: Aufgrund der höheren Metall-Ionen-Konzentration in der Lösung ist der Abscheidungsdruck hier größer als der Lösungsdruck. Die Elektrode lädt sich dadurch weniger stark negativ auf, weshalb die Elektrode in dieser Halbzelle das höhere Elektrodenpotenzial aufweist.
In Konzentrationszellen dieses Typs bildet die Halbzelle mit der niedrigeren Elektrolytkonzentration deshalb die Anode (Ort der Oxidation, Minus-Pol) und die Halbzelle mit der höheren Elektrolytkonzentration die Kathode (Ort der Reduktion, Plus-Pol).
Weiteres
Stellt man zwischen den Polen einer Kupfer-Konzentrationszelle eine leitende Verbindung her, so ist die Halbzelle mit der verdünnteren Lösung also die so genannte Donator-Halbzelle. Kupfer-Atome werden oxidiert und gehen als Kupfer-Ionen in Lösung. Die Halbzelle mit der konzentrierteren Lösung ist dementsprechend die Akzeptor-Halbzelle. Hier werden Kupfer-Ionen zu Kupfer-Atomen reduziert. Bei laufendem Betrieb dieser Konzentrationszelle wird der Konzentrationsunterschied zwischen den Halbzellen allmählich kleiner und die Spannung nimmt langsam ab. Der Stromfluss endet, wenn sich innerhalb der jeweiligen Halbzelle ein Gleichgewicht zwischen Lösungsdruck und Abscheidungsdruck eingestellt hat und in beiden Halbzellen die gleiche Ionenkonzentration vorliegt.
Der quantitative Zusammenhang zwischen Elektrodenpotential und Ionenkonzentration wurde von Walter NERNST untersucht. Seine Ergebnisse hat er 1889 in der NERNST-Gleichung zusammengefasst. Für galvanische Halbzellen gilt bei 25°C:
z entspricht der Anzahl der übertragenen Elektronen je Teilchen. Der Term c(Ox) / c(Red) beschreibt den Massenwirkungsgesetz-Term der Oxidation oder Reduktion. Dabei sollen die Reaktionspartner der oxidierten Reaktionsseite im Zähler stehen. Die Spannung der Gesamtzelle berechnet sich nach der Anwendung der NERNST-Gleichung für beide Halbzellen im Anschluss wie folgt:
Wendet man die NERNST-Gleichung auf eine Metall-Metallionen-Halbzelle an, so entsprechen die Metallionen den oxidierten Teilchen (Ox) und die Metallatome den reduzierten Teilchen (Red). Beispielsweise lautet die NERNST-Gleichung für eine Cu/Cu2+-Halbzelle:
Die Kupferatome liegen in Form einer festen Elektrode vor. Für nicht gelöste Feststoffe wird eine Konzentration von 1 eingesetzt, da ein Feststoff keine Konzentration haben kann. Damit vereinfacht sich die NERNST-Gleichung wie folgt:
Dasselbe gilt auch für Gase: Auch hier wird eine Konzentration von 1 mol/L angenommen.
Beispiel: Berechnung Redoxpotential
Weiteres
Im folgenden Beispiel berechnen wir das Redoxpotential des Redoxpaares Cu/Cu2+ mit c(Cu2+) = 0,01 mol/L.
Das Redoxpotential des Redoxpaares Cu/Cu2+ mit c(Cu2+) = 0,01 mol/L beträgt 0,281 V und ist damit geringer als sein Standard-Redoxpotential.
Beispiel: Spannung berechnen
Weiteres
Zur Erinnerung: Beim Aufstellen des Massenwirkungsgesetz-Terms wird die Konzentration des Wassers nicht in den Term aufgenommen.
Die galvanische Zelle weist eine Spannung von ca 2 V auf.
Übung
- Notieren Sie zu den nachfolgenden Reaktionsgleichungen die Nernst-Gleichung:
- Fe3+ + e– ⇌ Fe+
- H2O2 + 2e– ⇌ 2 OH–
- SO42- + 2 H3O+ + 2e– ⇌ SO32- + 3 H2O
- 4 OH– ⇌ O2 + 2 H2O + 4e–
- Notieren Sie zu den nachfolgenden Zelldiagrammen die Reaktionsgleichungen für die an den Elektroden ablaufenden Reaktionen und berechnen Sie die Halbzellen-Potentiale sowie die Zellspannung.
- Ag / Ag+ (0,001 mol/L) // Ag+ (0,1 mol/L) / Ag (0,12 V)
- Zn / Zn2+ (0,0001 mol/L) // Pb2+ (0,1 mol/L) / Pb (0,72 V)
- H2 / H3O+ (0,001 mol/L) // Ag+ (0,1 mol/L) / Ag (0,62 V)
- Li / Li+ (0,2 mol/L) // Cu2+ (0,5 mol/L) / Cu (3,41 V)
- Fe2+ (0,1 mol/L) / Fe3+ (0,05 mol/L) // Au3+(0,2 mol/L) / Au (0,734 V)