Aufgaben
- Sortieren Sie die Bausteine bzw. Reaktionsschritte in M1 so, dass daraus ein sinnvoller Reaktionsmechanismus für eine Veresterung entsteht. Vergleichen Sie anschließend mit der Lösung.
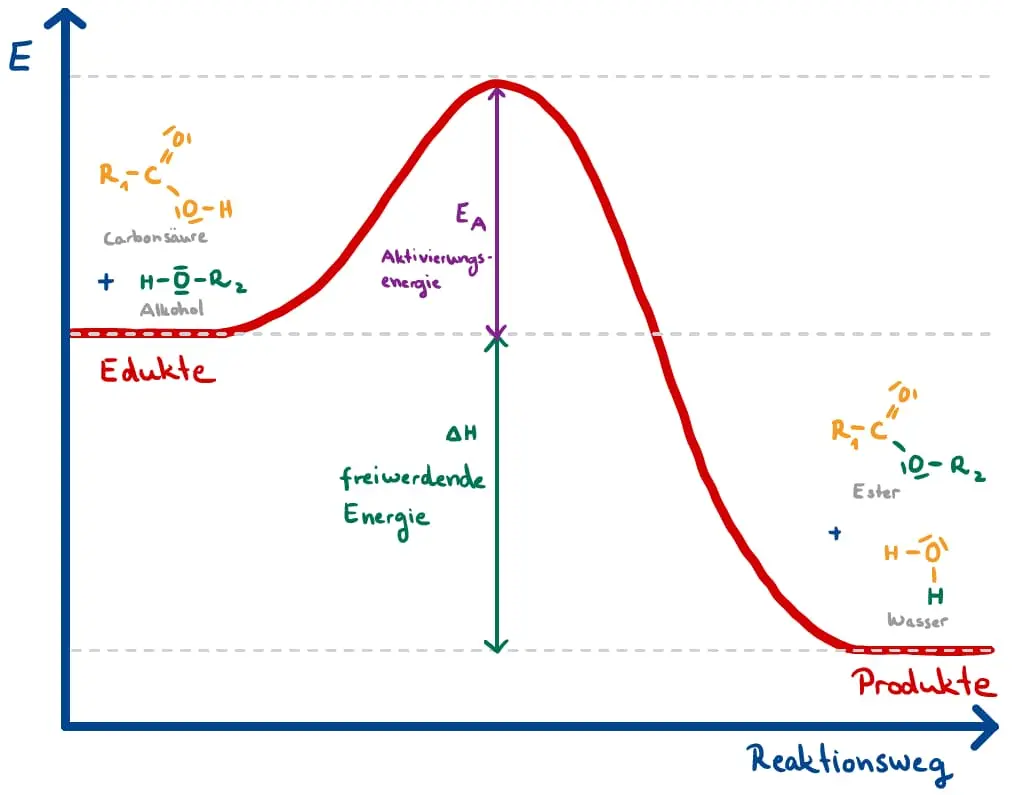
- Erläutern Sie mit Hilfe von M3, dass der Begriff Katalysator auf die zugegebene Schwefelsäure zutrifft. Skizzieren Sie in Abb. 1 die Katalysatorwirkung auf den Reaktionsverlauf ein.
- Beschreiben Sie den Reaktionsmechanismus Schritt für Schritt mit Hilfe der Formulierungshilfen in M2.
Bausteine für einen Reaktionsmechanismus
Mit Hilfe eines Reaktionsmechanismus lässt sich der Ablauf einer chemischen Reaktion in Form von Zwischenschritten näherungsweise darstellen. Verknüpfte Zwischenschritte können mit einem einfachen Reaktionspfeil verbunden sein. Nachfolgend sind Bausteine für einen Reaktionsmechanismus der Veresterung dargestellt. Sie sind durcheinandergeraten und auch die Reaktionspfeile fehlen. Bekommst Du hier Ordnung rein?
Weiteres
Formulierungshilfen
Die nachfolgenden Begriffe dienen als Hilfe zur Beschreibung eines Reaktionsmechanismus.
Weiteres
Fachbegriffe
- Carbonsäure
- Alkohol
- Katalysator
- Proton
- Carboxylgruppe / Carbonsäure-Gruppe
- Hydroxy-Gruppe
- C-O-Doppelbindung
- Carbenium-Ion
- Oxonium-Ion
- Carbonyl-C-Atom
- Elektronen
- freies Elektronenpaar des Sauerstoffatoms
- Eliminierung(sreaktion)
- Addition(sreaktion)
- Wasserstoffbrückenbindung
- positive Ladung
- Ester
Verben
- reagieren
- dienen als
- protonieren
- sich bilden
- anlagern
- angreifen
- beschleunigen
- entstehen
- tragen
- wandern
- verschieben
- abspalten
- sich zurückbilden
Eigenschaften
- positiv geladen
- doppelt gebunden
- elektrophil
- nucleophil
- aktiviert
- partiell negativ/positiv geladen
- intramolekular
- instabil
Katalysator
Weiteres
Der Begriff Katalysator bezeichnet in der Chemie einen Stoff, der die Reaktionsgeschwindigkeit (…) erhöht, ohne dabei selbst verbraucht zu werden. Ein Katalysator nimmt an einer chemischen Reaktion unter Bildung einer intermediären Stufe (Zwischenstufe) mit den Reaktanten (Reaktionsteilnehmern) teil, aus dem der Katalysator nach Entstehung des Produkts unverändert freigesetzt wird. Ein Katalysator kann diesen so genannten Katalysezyklus viele Male durchlaufen.1
Weiteres
Energiediagramm zu einer Estersynthese. 2
Mesomerie
Weiteres
Als Mesomerie wird in der Chemie ein Phänomen bezeichnet, bei dem die Bindungsverhältnisse in einem Molekül oder Ion nicht durch eine einzige Strukturformel, sondern nur durch mehrere Strukturformeln dargestellt werden können. Solche Strukturformeln werden auch als Grenzformeln bezeichnet. Keines dieser Grenzformeln beschreibt die Verteilung der Elektronen in ausreichender Weise. Sie stellen lediglich ne Art Momentaufnahme dar. Die Grenzformeln werden durch ein Mesomeriepfeil (Doppelpfeil) miteinander verknüpft. Je mehr Grenzformeln für ein Molekül oder Ion aufgestellt werden können, desto stabiler ist es.
Weiteres
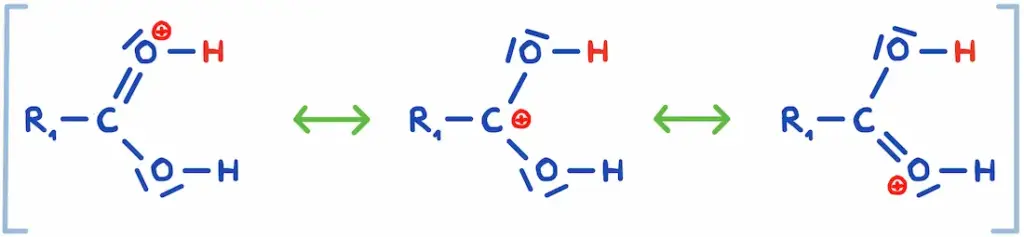
Nachfolgend ist die Mesomerie an einem Beispiel dargestellt. Mit Hilfe der Grenzformeln ist ersichtlich, dass bestimmte Elektronen und die positive Ladung nicht an einem Ort lokalisiert sind, sie sind vielmehr delokalisiert.
Drei mesomere Grenzformeln am Beispiel einer Zwischenstufe bei der Veresterung. 2
Weitergedacht
- Erkläre mit Hilfe von M4, was man unter dem Begriff Mesomerie versteht und ordne Abb. 1 als Baustein deinem Reaktionsmechanismus gedanklich zu. Erweitere deine Beschreibung aus Aufgabe 2 um deine neuen Erkenntnisse rund um die Mesomerie.
- Übe deine neu erworbenen Kenntnisse mit M5.