Gedanken vorab
Lesetipp
Hier ein Lesetipp zur Entstehungsgeschichte des Periodensystems für alle, die es genau wissen wollen.
Hilfe bei Fachtexten
Du verstehst einen Fachtext nicht vollständig? Ich kann ihn in einfacher Sprache1 ausgeben.
Einwicklung erster Vorstellungen
Rückblick
Erinnerst Du dich? Um die Jahrhundertwende zum 19. Jahrhundert hatte man erste konkrete Vorstellungen von Atomen entwickelt, die Zusammensetzung von Stoffen beschreiben und das Gesetz von der Erhaltung der Masse erklären können.
Rückblick: von der Wort- zur Formelgleichung2
Zur Erinnerung
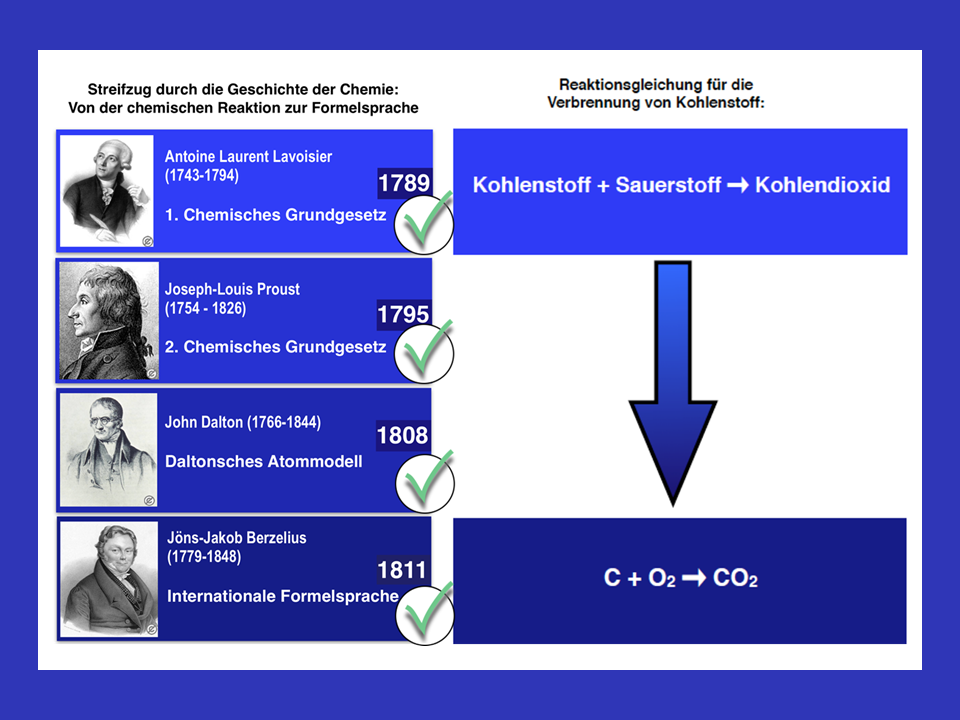
Antoine de Lavoisier (1743–1794) gilt als Begründer der modernen Chemie. Er formulierte das Gesetz der Massenerhaltung (auch: 1. chemisches Grundgesetz), das besagt:
„Bei einer chemischen Reaktion bleibt die Gesamtmasse der reagierenden Stoffe und der Produkte stets konstant.“
Joseph Louis Proust (1754–1826) war der entscheidende Chemiker, der das sogenannte Gesetz der konstanten Proportionen (auch: Gesetz der definierten Proportionen) formulierte. Dieses Gesetz stellt das 2. chemische Grundgesetz dar und lautet:
„In einer chemischen Verbindung sind die Elemente stets in einem bestimmten Massenverhältnis enthalten, unabhängig davon, wie die Verbindung hergestellt wurde oder woher die Ausgangsstoffe stammen.“
Moderne, vereinfachte Übersicht über die Idee Daltons3
Dalton griff diese experimentellen Befunde auf und interpretierte sie revolutionär: Er stellte die Hypothese auf, dass Materie aus kleinsten Teilchen besteht – den Atomen. Sein Modell erklärt das Gesetz der Massenerhaltung (weil Atome bei Reaktionen nicht „verschwinden“) und das Gesetz der konstanten Proportionen (weil Verbindungen durch feste, atomare Zahlenverhältnisse gebildet werden).
Daltons Arbeit verband also direkt die Erkenntnisse von Lavoisier und Proust zu einer Theorie, die chemisches Geschehen erstmals auf atomarer Ebene beschrieb.
Dalton nahm an, dass es nur wenige elementare Stoffe gibt, die jeweils aus einer einzigen Sorte Atome bestehen, während die meisten anderen Stoffe als Verbindungen aus den Atomen verschiedener Elemente aufgebaut sind.
Jöns Jakob Berzelius (1779–1848) spielte eine zentrale Rolle als Systematisierer in der Chemie des 19. Jahrhunderts und verbindet die Arbeiten von Lavoisier, Proust und Dalton mit der weiteren Entwicklung der chemischen Grundgesetze:
Einführung der chemischen Symbolik: Berzelius führte das heute noch gebräuchliche System von chemischen Symbolen und Formelschreibweisen ein.
Systematische Bestimmung der Atommassen: Berzelius bestimmte mit hoher Genauigkeit die relativen Atommassen zahlreicher Elemente und schuf so eine sichere Datengrundlage für die entstehende Atomtheorie (Dalton) und für spätere Periodensysteme.
Beleg und Bestätigung der Grundgesetze: Durch seine exakten Analysen bestätigte er experimentell die Gesetze von Lavoisier (Massenerhaltung) und Proust (konstante Proportionen) und wies nach, dass chemische Verbindungen tatsächlich in ganz bestimmten Massenverhältnissen auftreten.
Dass hier zuvor ausschließlich männliche Forscher genannt werden, kann aus heutiger Sicht hinterfragt werden. „Der Gedanke, dass [z. B.] Marie-Anne [de Lavoisier] Einfluss auf die Forschungen ihres Mannes genommen hat, […] [ist] nicht ganz abwegig“4
Auf der Suche nach Zusammenhängen
Chemiebücher der damaligen Zeit wurden ständig überarbeitet, da man immer mehr und genauer Stoffe, deren Eigenschaften und Zusammensetzungen untersuchte. Dabei erkannte man auch, dass es Gruppen von Elementen gab, die sich in Reaktionen ähnlich verhielten.
Ausschnitt aus einem Buch des Schweden Berzelius von 1825, übersetzt von F. Wöhler, einem ebenso berühmten Chemiker und Schüler von Berzelius.5
Ein Ordnungssystem entsteht
Bereits 1864 erkannte Lothar Meyer bei den Eigenschaften von Elementen in gewissen Abständen Regelmäßigkeiten, wenn er sie nach dem Atomgewicht ordnete. 1869 gelang dann Dmitri Mendelejew ein Durchbruch. In seiner Arbeit „Versuch eines Systems der Elemente, begründet auf deren Atomgewichten“ findet sich zum ersten Mal der Ausdruck „das Periodensystem der Elemente.“6
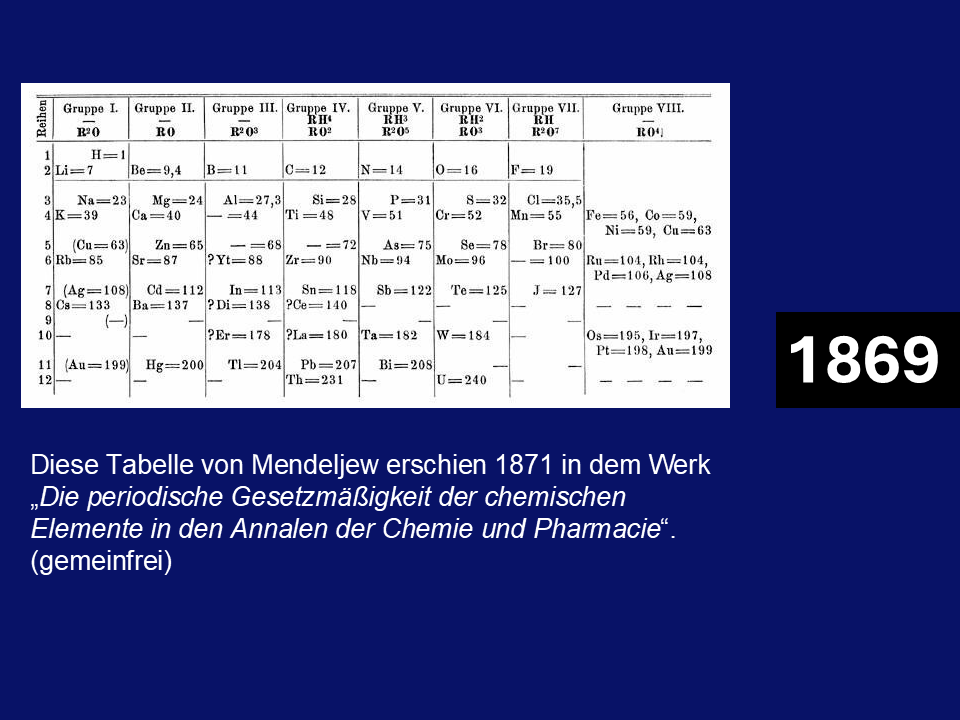

Begründer des „PSE“ und eine Tabelle von Mendelejew.7
Wir wollen das nachstellen
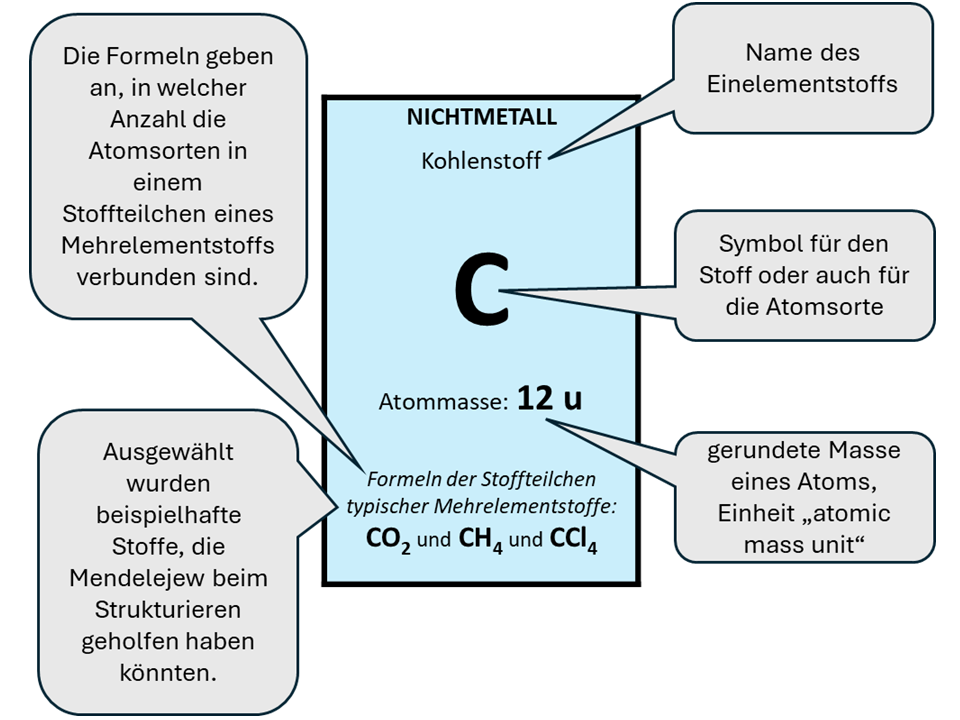
Mendelejew ordnete die Elemente sowohl nach Atomgewichten als auch im Bezug auf ihre Eigenschaften. Dazu fertigte er Karten für alle damals bekannten 63 Elemente mit chemischen Symbolen und Atomgewichten an und begann, eine Art „chemische Patience“ zu legen.8
Lass uns dies auch einmal machen. Und zwar analog, genau wie Mendelejew!
Wir begeben uns auf Mendelejews Spuren
Weiteres
Was denkst Du? Wonach können wir die Elemente mit den Informationen auf unseren Karten sortieren, wenn wir ähnlich vorgehen wollen wie Mendelejew?
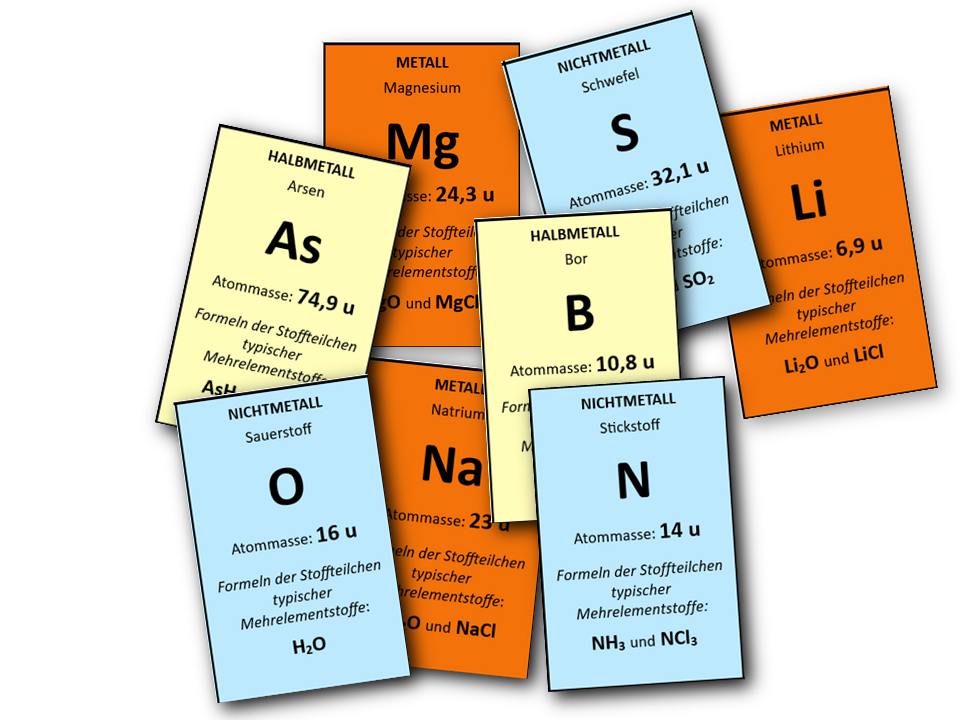
Einige ausgewählte Karten.10
Wir beginnen gemeinsam
Weiteres
Ordne alle Elementkarten nach zunehmender Atommasse in einer langen Reihe.
Der Beginn einer Sortierung.10
Suche Ähnlichkeiten
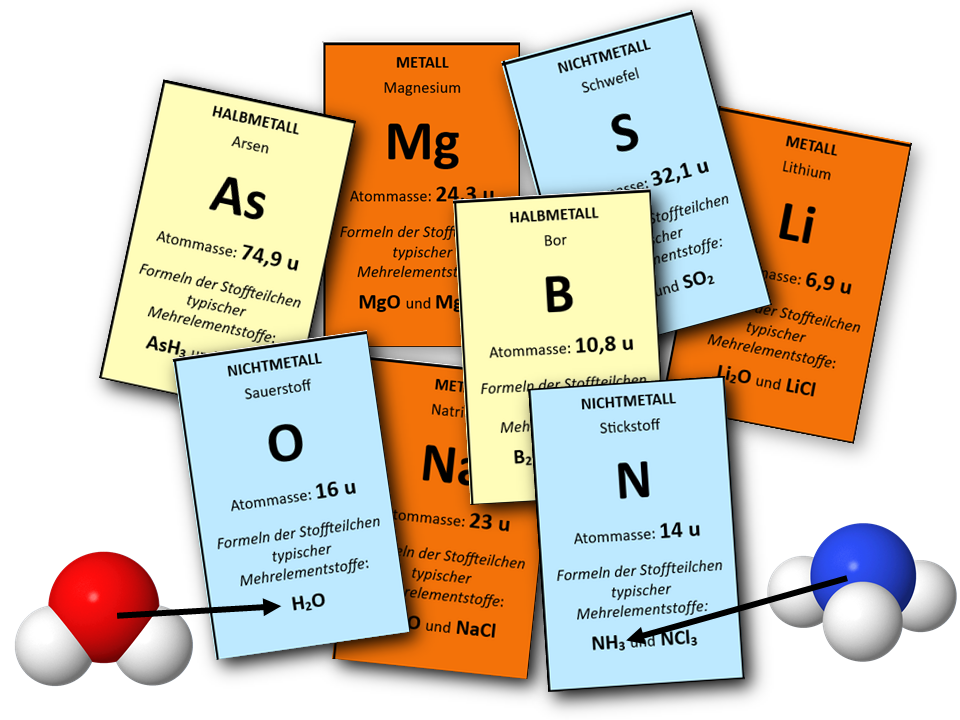
Ziehe die Karte für Lithium ein Stückchen aus der Reihe heraus. Überprüfe, ob es in der langen Reihe Elemente gibt, die Mehrelementstoffe mit anderen Elementen im gleichen Verhältnis wie Lithiums bilden.
Mache das Gleiche für Beryllium, Bor, Kohlenstoff etc. Was fällt dir auf?
Die Bedeutung von Periodizität.11
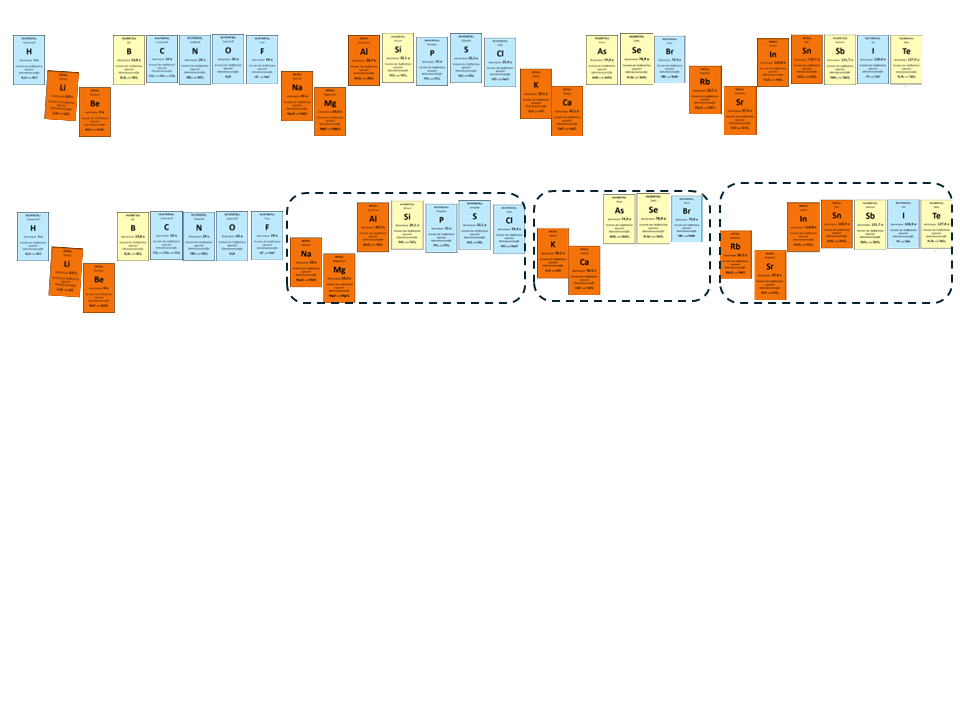
Jetzt bis du dran: eine Sortieraufgabe
- Ordne die Elementkarten aus dem Set so, dass sie sowohl nach zunehmender Atommasse als auch nach ähnlichen Verhältnisformeln der Verbindungen sortiert sind.
Aufgaben nach dem Puzzle
- Benenne die Ordnungskriterien, nach denen die Elemente im Periodensystem angeordnet sind.
- Erkläre die Bedeutung des Worts „Periodensystem“.
- Stellen wir uns vor, in den Lücken fehlen noch Elemente, die man noch nicht entdeckt hatte. Nennen wir sie X und Y. Stelle eine begründete Vermutung auf, was die Forscher bezüglich Metall/Halbmetall, der Formeln oder der Atommassen herausfanden.
- Beschreibe die „interessante“ Stelle erkläre, inwiefern sie zeigt, dass es ein „Hauptordnungskriterium“ gibt.
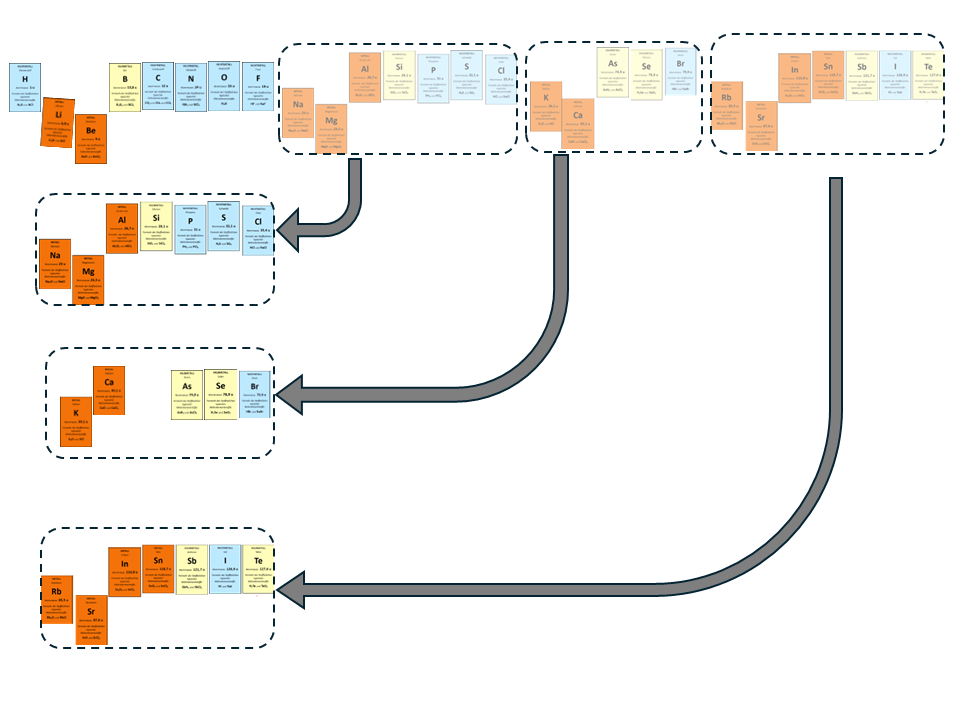
Das fertige Puzzle, Lücken, interessante Stelle
Es soll ein Raster ergeben. Senkrecht sind immer „Familien“ von Elementen mit ähnlichen Eigenschaften bzw. ähnlichen Verbindungen der Elemente mit anderen Elementen.
Von oben nach unten und von rechts nach links soll die Atommasse der Elemente steigen.
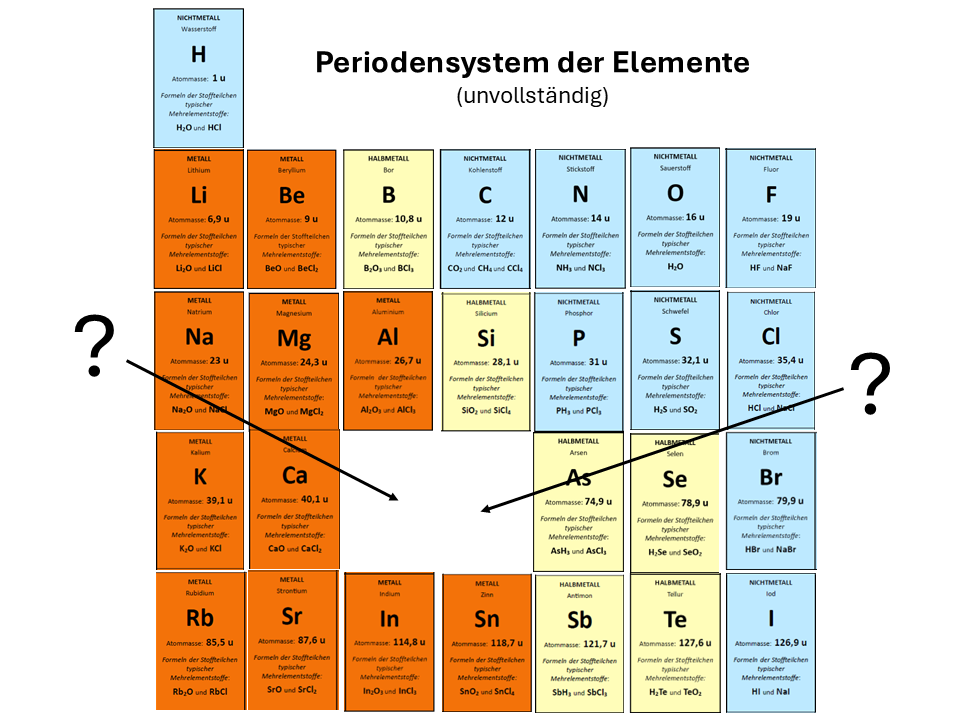

Was kann man hier vermuten?12
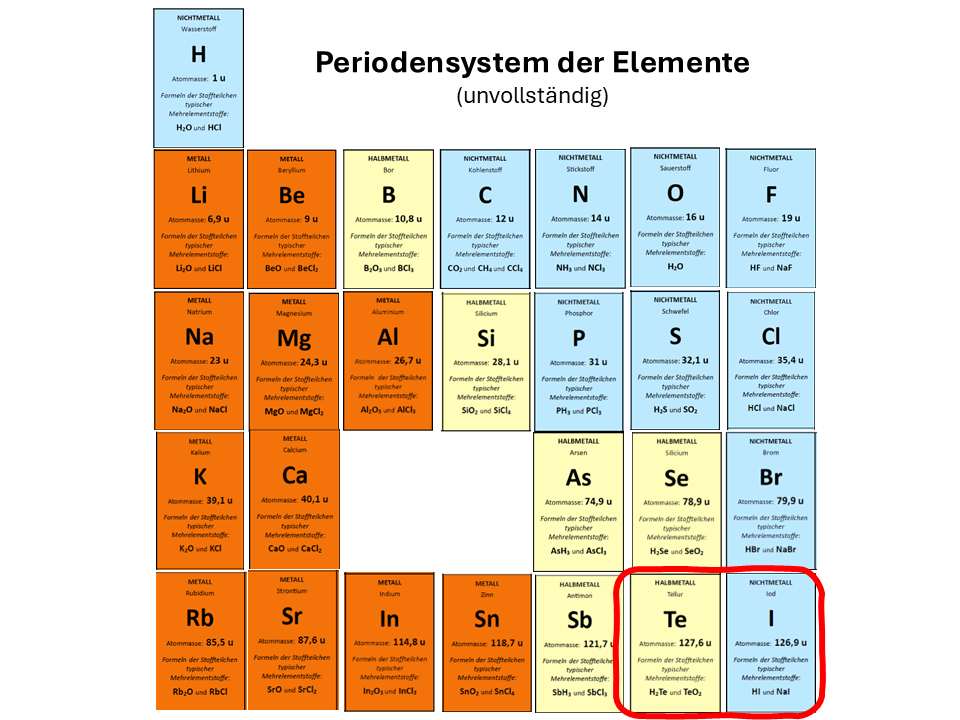

Diese interessante Stelle sagt viel aus.12