Ein kurzer historischer Rückblick
Schon länger bekannt
Schon in den Jahren ab 1861 untersuchten die Franzosen Marcelin Berthelot und Péan de Saint-Gilles die Reaktion von Säuren mit Alkoholen zu Estern und umgekehrt und erkannten, dass beide Systeme auf einen gemeinsamen Gleichgewichtszustand hinauslaufen.
Wenig später bestimmen die Norweger Cato Guldberg und Peter Waage die Konzentrationen von Stoffe im Gleichgewicht, die sie damals noch „wirkende Massen“ nannten und belegen den Gedanken des sich einstellenden Gleichgewichts.1
Zunächst deutete man diesen Zustand allerdings als eine Art Stillstand. Man dachte, die Reaktionen kommt zum Erliegen.
Weiteres
Zwei norwegische Chemiker sprechen von „wirkenden Massen“2
Weiteres
Durch die Arbeiten von Jacobus van ’t Hoff, setzte sich dann Ende des 19 Jahrhunderts die heute zentrale Vorstellung durch: Ein chemisches Gleichgewicht ist dynamisch. Auch im Gleichgewicht laufen Hin- und Rückreaktion weiter ab – allerdings mit gleicher Geschwindigkeit.
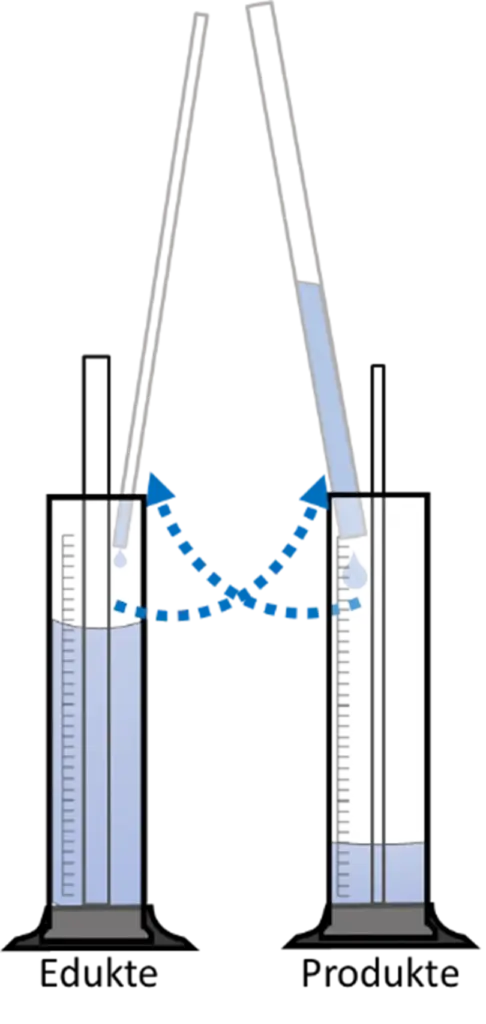
Wie man sich einen solchen Zustand vorstellen kann, ist auf den ersten Blick vielleicht nicht leicht zu erkennen. Gerade weil sich äußerlich nichts zu verändern scheint, bleibt die zugrunde liegende Dynamik zunächst unsichtbar. Ein Modellversuch mit zwei Messzylindern kann dabei helfen, das dynamische chemische Gleichgewicht anschaulich begreifbar zu machen.
Aufgaben
- Führen Sie den Modellversuch gemäß der Anleitung in Partnerarbeit durch.
- Notieren Sie Ihre Ergebnisse in der Auswertungshilfe.
- Verschieben Sie die senkrechte Linie und markieren Sie im Grafen auf diese Weise die Stelle, an der ihrer Meinung nach das Gleichgewicht erreicht ist.
- Machen sie einen Screenshot der Auswertung.
- Erklären Sie unter Verweis auf das Modellexperiment, was man unter einem dynamischen Gleichgewicht versteht.
Modellversuch zur Dynamik des chemischen Gleichgewichts
Weiteres
Viele Reaktionen verlaufen hin und zurück:
Die Geschwindigkeiten der Hin- und Rückreaktion
unterscheiden sich zunächst. Aber irgendwann verlaufen Hin- und Rückreaktion gleich schnell. Es stellt sich ein sogenanntes dynamisches Gleichgewicht ein.
Warum man dies ein dynamisches Gleichgewicht nennt, soll in einem Modellversuch veranschaulicht werden.
Materialien
- 2 Messzylinder 50 mL
- 2 Glasrohre
- mit unterschiedlichem Durchmesser
Chemikalien
-
Wasser
- mit Lebensmittelfarbe eingefärbt
Aufbau und Durchführung
- Der Messzylinder, der modellhaft für die „Edukte“ steht, wird mit 50 mL gefärbtem Wasser befüllt.
- Nun wird 20 Mal aus diesem Messzylinder mit einem Glasrohr Flüssigkeit entnommen, indem man das Glasrohr auf den Boden des Messzylinders stellt und das obere Ende des Glasrohrs mit dem Daumen verschließt. Die Flüssigkeit wird in den Messzylinder „Produkte“ überführt.
- Gleichzeitig(!) wird 20 Mal mit dem zweiten Glasrohr die Flüssigkeit vom zunächst leeren Messzylinder „Produkte“ in den Messzylinder „Edukte“ befördert.
- Wichtig ist, dass für jeden „Flüssigkeitsaustausch“ immer das gleiche Rohr in den gleichen Zylinder gestellt wird. Beispielsweise wird immer das Rohr mit dem größeren Durchmesser im Zylinder „Edukte“ gefüllt und im Zylinder „Produkte“ entleert.
Entsorgen und Aufräumen
-
Reste in den Ausguss geben und mit viel Wasser nachspülen.
-
Alle verunreinigte Labormaterialien spülen.
-
Alle Materialien an ihren Ursprungsort zurückstellen.
Auswertungshilfe
Weiteres
Tiefergehende Auswertung
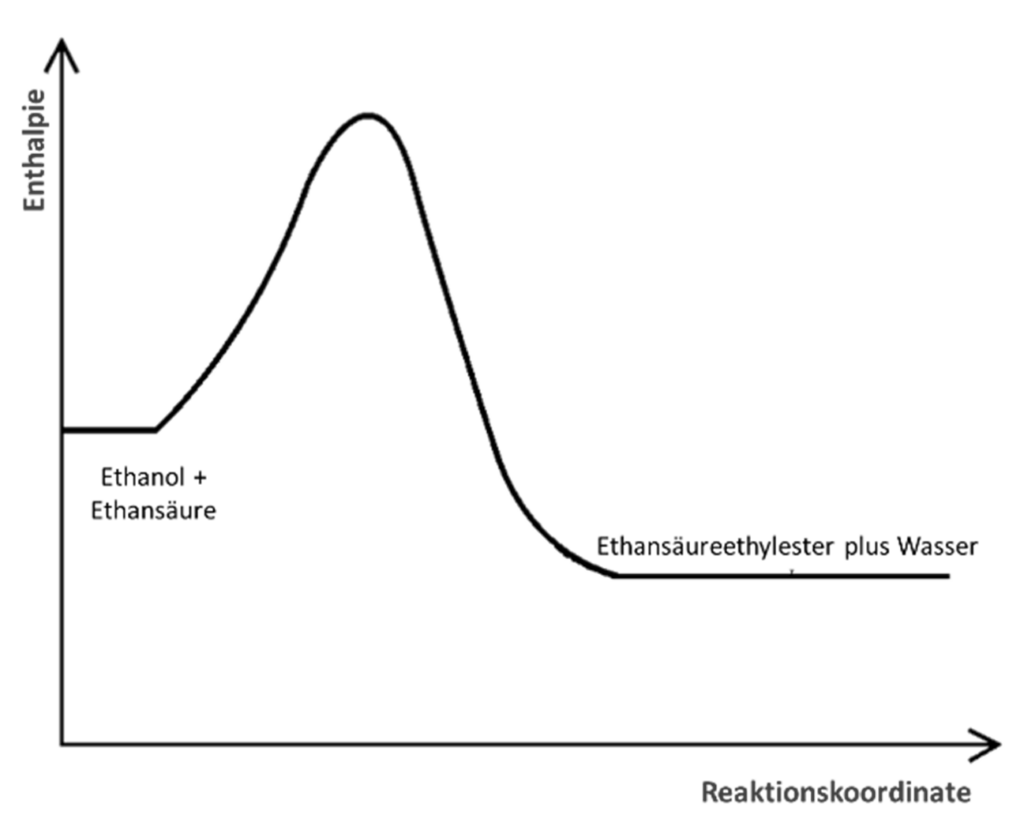
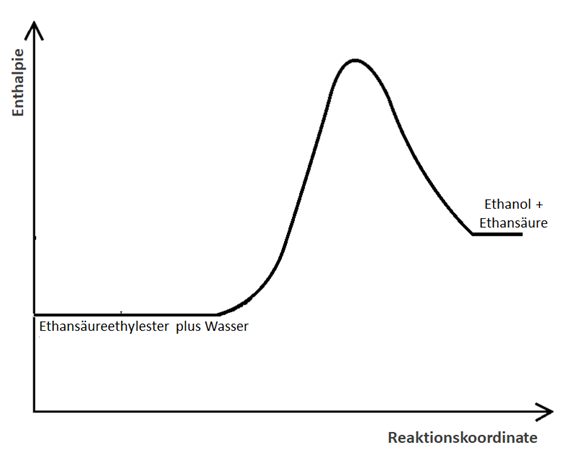
- Übertragen Sie das Modell auf den Versuch zur Veresterung bzw. Esterspaltung. Ergänzen Sie dazu folgende Satzanfänge:
- Der Flüssigkeitsspiegel in Messzylinder Edukte steht für …
- Der Flüssigkeitsspiegel im Messzylinder Produkte steht für
- Die Flüssigkeitsmenge in den Rohren entspricht
- Der Durchmesser des … Rohres symbolisiert …
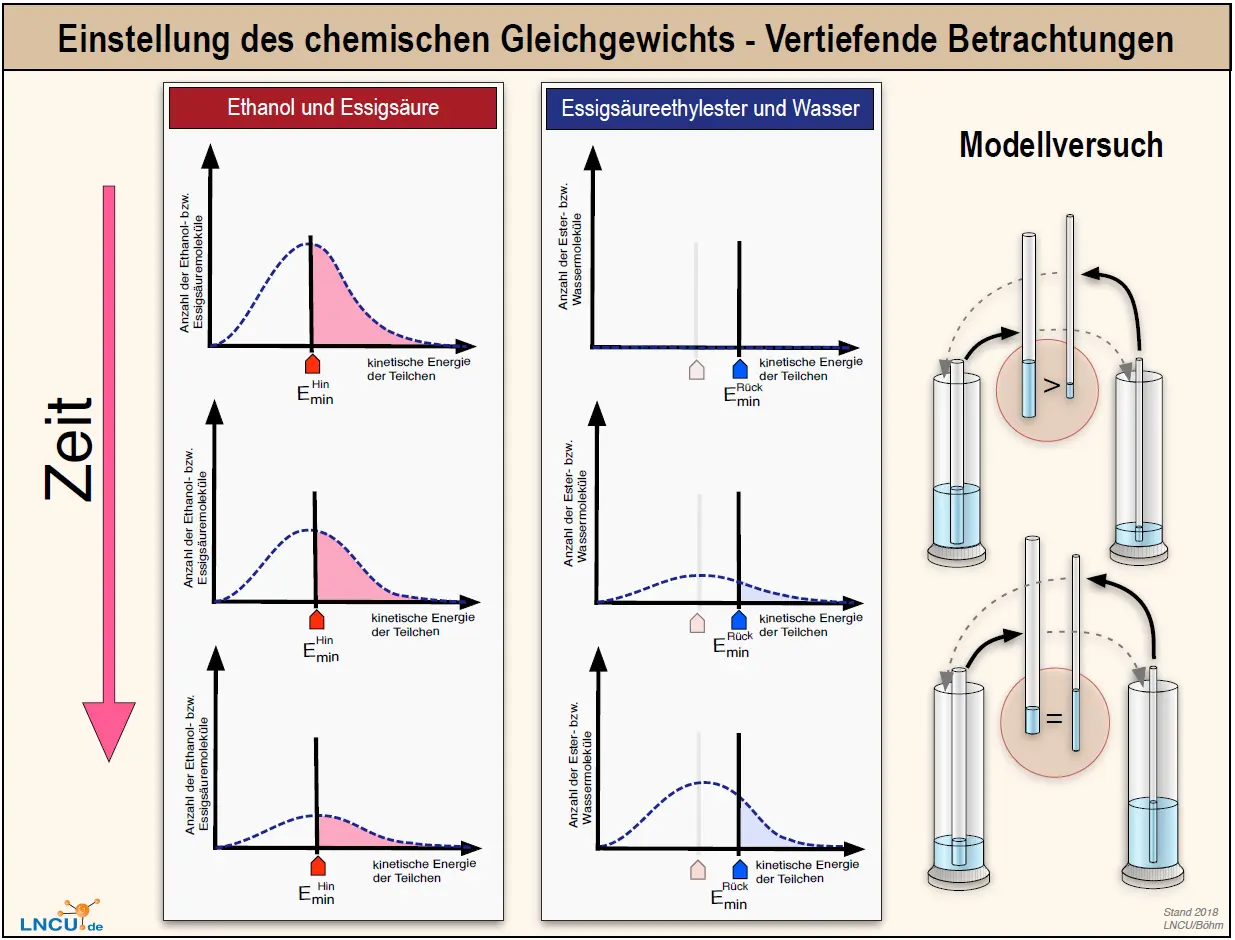
- Erklären Sie, warum im Gleichgewichtszustand die Konzentration der Edukte und Produkte nicht gleich sein kann. Nutzen Sie dafür M3.
- Stellen Sie begründete Vermutungen auf, welche Versuchsergebnisse man erhält, wenn man die Glasrohre vertauscht nutzen würden. Prüfen Sie Ihre Vermutung ggf. anhand von Messergebnissen anderer Gruppen.
Weitergehende Gedanken
Weiteres
Dann vergleiche die Höhen und die farbig markierten Flächen unter den Kurven und erläutere ihre Bedeutung.
Boltzmann-Verteilung und Stechheberversuch im Zusammenhang 3