Verändert sich die Reaktionsgeschwindigkeit mit der Größe der Oberfläche?
Weiteres
Kleine Holzspäne lassen sich schneller entzünden als ein dicker Holzstamm. Ein Medikament in Tablettenform löst sich langsamer im Magen auf als das gleiche Medikament in Pulverform. Die Oberfläche eines Feststoffes scheint einen Einfluss auf die Reaktionsgeschwindigkeit zu haben.
Weiteres
Im Folgenden beantworten wir die Frage exemplarisch für die Bildung von Wasserstoff bei der Reaktion von Salzsäure mit Magnesium:
und erklären die Beobachtungen mit der sogenannten Stoßtheorie auf Teilchenebene.
Aufgaben
- Formulieren Sie eine Erwartung bezüglich der Geschwindigkeit der Reaktion von Magnesium mit Salzsäure, wenn man Oberfläche des Feststoffes vergrößert.
- Schlagen Sie einen prinzipell geeigneten Versuch vor, ihre Erwartungshaltung zu prüfen und benennen Sie die wesentlichen Aspekte, die es zu beachten gilt.
- Führen Sie den versuch gemäß der Anleitung V1 durch und filmen Sie das Experiment dabei, um es nachfolgend auszuwerten.
- Werten Sie ihre Ergebnisse auch unter Verwendung von M2 aus.
Kommt es auf die Größe der Oberfläche an?
Materialien
- Schutzbrille
- 2 Spritzen (12 mL)
- 2 Spritzen (30 mL)
- Verbinder luer-lock w-w
- Rückschlagventil luer-lock
- alternativ: 3-Wegehahn zum Verschließen
- Becherglas
-
Waage
- 0,001 g genau
- 2 Klammern mit Magnet
- fakultativ zum Fixieren während der Filmaufnahme
Chemikalien
-
Salzsäure (1 mol / L)
- aus dem Becherglas in die 10 mL Spritze aufziehen
-
Magnesiumband, gefaltet ca. 2 cm
- wiegen!
-
Magnesiumspäne
- in etwas die gleiche Masse wie das Band
Hinweise
Haben Sie keine genügend genaue Waage, schätzen Sie etwa gleich viele Mengen Magnesiumband und -späne ab.
Es entsteht Wasserstoff – von Zündquellen fernhalten!
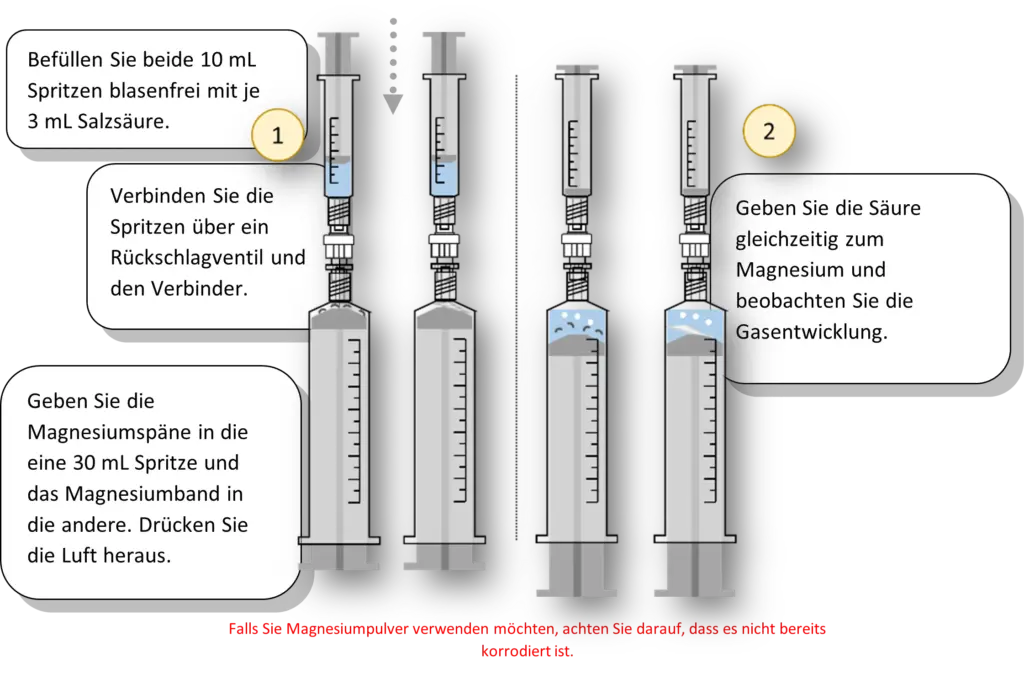
Aufbau und Durchführung
Skizze Aufbau und Beschreibung der Durchführung1
Videografie des Versuch
Videografie, falls der Versuch nicht durchgeführt werden kann2
Entsorgen und Aufräumen
-
Alle verunreinigte Labormaterialien spülen.
-
Alle Materialien an ihren Ursprungsort zurückstellen.
-
Restliche Lösung in den Sammelbehälter geben. Entstandenen Wasserstoff im Abzug oder am offenen Fenster in die Luft entlassen.
Die sogenannte Stoßtheorie
Modell zur Stoßtheorie an festen Oberflächen
Stoffe müssen zusammenkommen, um zu reagieren.
Auf Teilchenebene bedeutet dies, dass Atome, Ionen oder Moleküle zusammenstoßen müssen, damit Reaktionen stattfinden können.
Die meisten der Reaktionen, die wir betrachten, finden in einer Phase statt und an ihnen sind dann entweder nur Gase oder Lösungen beteiligt.
Wenn sich Reaktanten aber in unterschiedlichen Phasen befinden, wenn also zum Beispiel einer der Stoffe eine Flüssigkeit und der andere ein Festkörper ist, ist die Reaktion auf ihre Grenzflächen beschränkt.
Vergrößert man die Oberfläche des Feststoffes, so finden auf Teilchenebene die Zusammenstöße, die für eine Reaktion notwendig sind, häufiger statt.
Weiteres
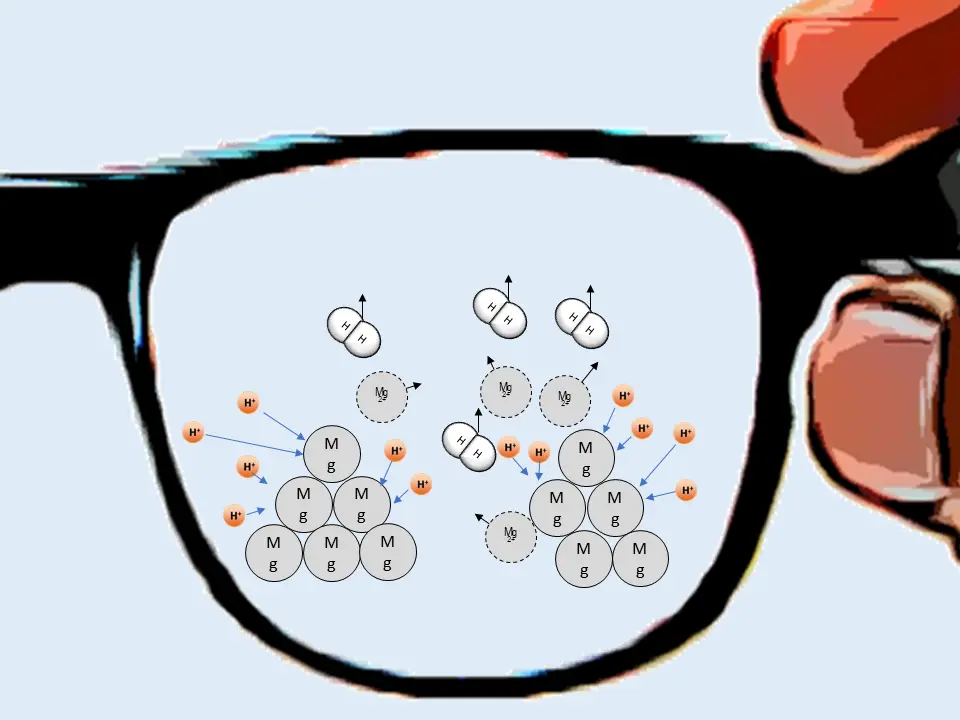
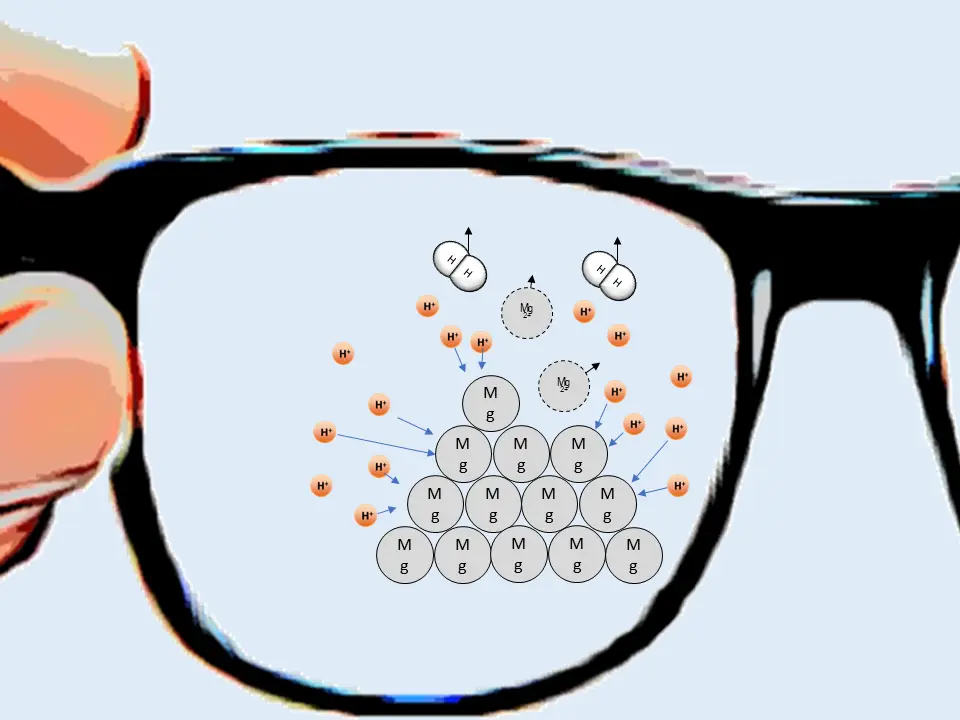
Modell des Versuchs auf Teilchenebene im Vergleich3
Hinweise:
- der blaue Hintergrund im vereinfachten Modell soll zeigen, dass es sich um eine Lösung handelt, in der die Ionen frei beweglich sind. Eine zusätzliche Darstellung der Wassermoleküle als Teilchen würde die Abb. überfrachten.
- Die Wasserstoff-Ionen (H+) sind demzufolge hier nicht als Oxonium-Ionen (H3O+) dargestellt