M1
Wir fassen zusammen
Weiteres
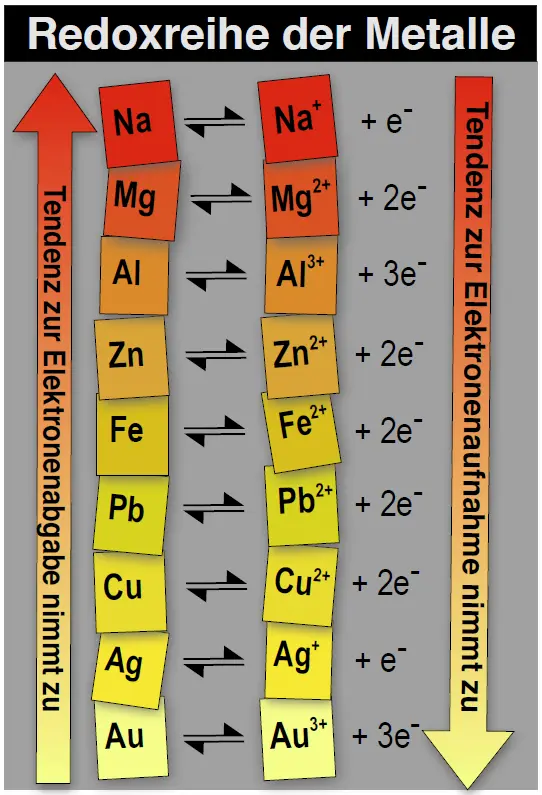
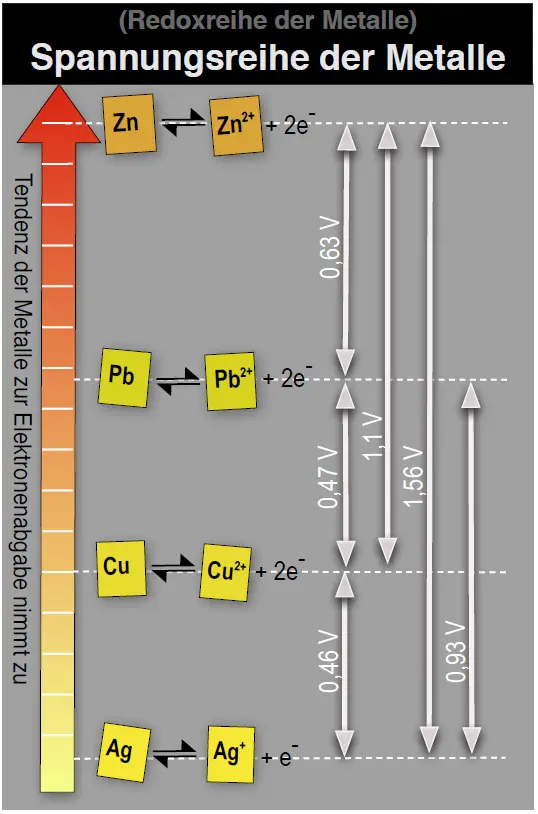
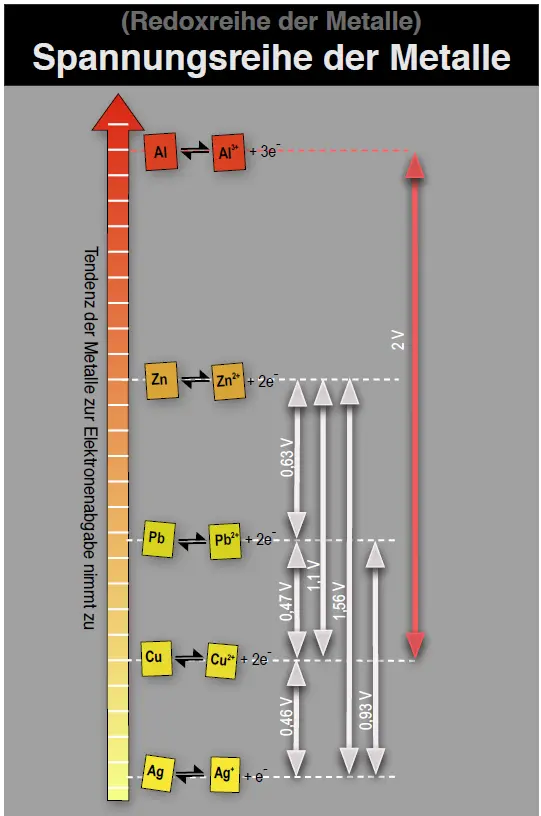
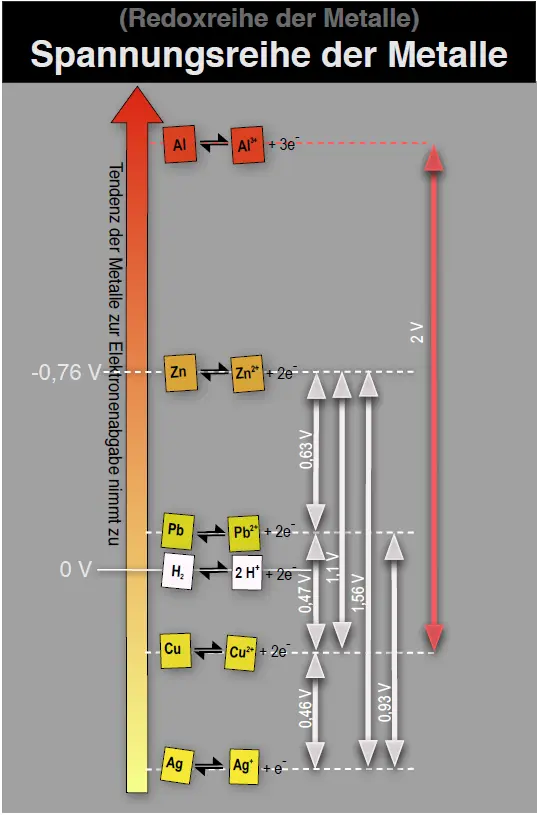
Wir überführen die Redoxreihe der Metalle in eine Spannungsreihe der Metalle.1
M2
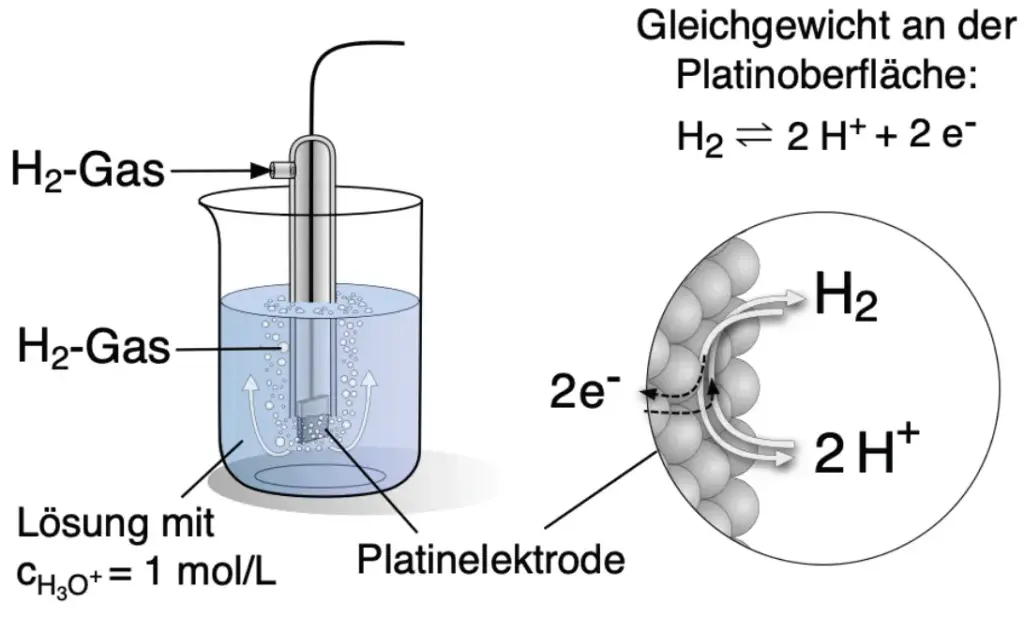
Die Wasserstoffnormalhalbzelle
Weiteres
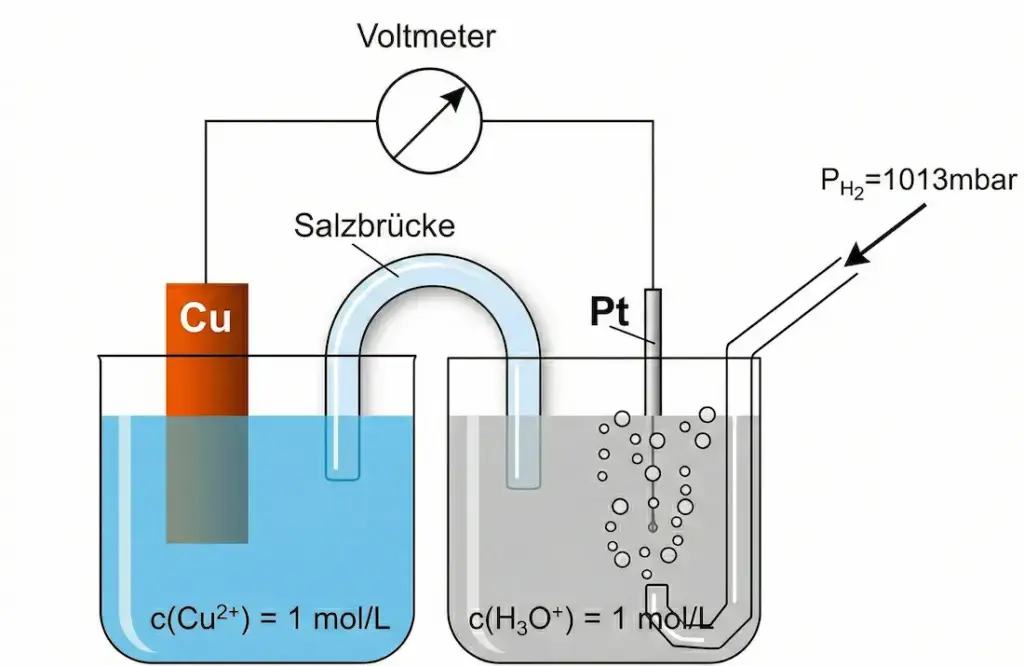
Links: Aufbau einer Wasserstoff-Elektrode. Rechts: Messung des Standardpotentials einer Kupfer-Halbzelle.2
V1
Messung der Spannung gegen eine Wasserstoff-Elektrode
Materialien
- Schutzbrille
- Filterpapier
- Zellblock
- Platin-Elektrode
- Spannungsmessgerät
- Multimeter
- 3 V Spannungsquelle
- dient zur Synthese von Wasserstoff an der Platin-Elektrode
- Schleifschwamm
- Alternativ Schmirgelpapier
Chemikalien
- Zink-Blech
- Kupfer-Blech
- Magnesium-Band
- Salzsäure 0,1 mol/L
- Zinksulfat 0,1 mol/L
- Kupfersulfat 0,1 mol/L
- Magnesiumsulfat 0,1 mol/L
Durchführung
- Oberflächenverunreinigungen auf den Metall-Blechen (Elektroden) abschmirgeln.
- Zwischen den Zellbock-Hälften doppellagig angefeuchtetes Filterpapier (= Diaphragma) legen.
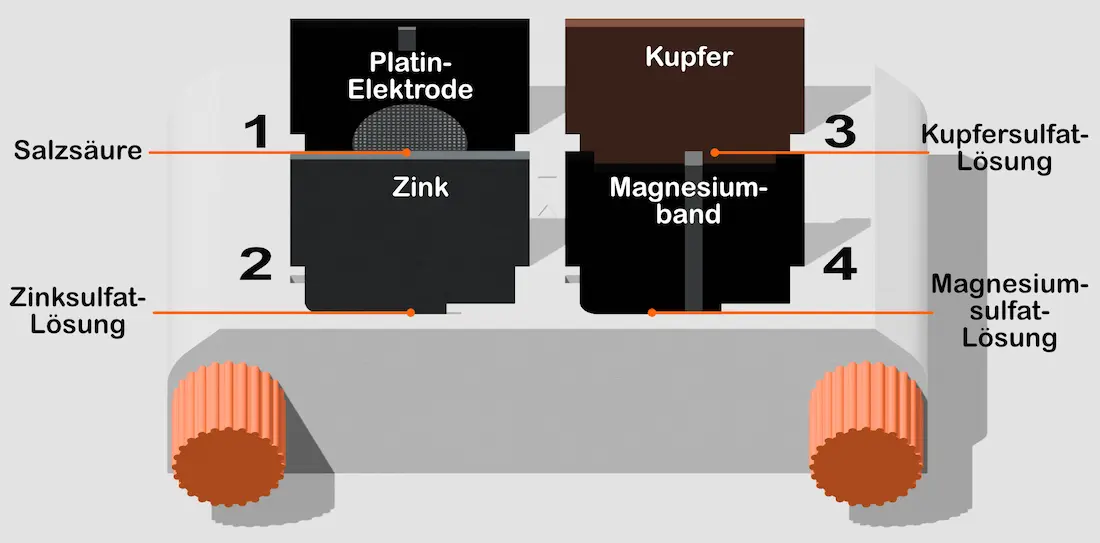
- 4 Halbzellen des Zellblocks bis zur inneren Markierung nach dem folgendem Schema befüllen:
Aufbau Zellblock.3
- Die Platin-Elektrode mit dem Minus-Pol der Spannungsquelle verbinden. Die gegenüberliegende Halbzelle mit dem Plus-Pol verbinden. An der Platinelektrode sollte eine leichte Gasentwicklung zu beobachten sein. Wenn dem so ist: Die Elektroden mit dem Spannungsmessgerät verbinden, Spannung messen und notieren.
- Den vorherigen Schritt mit den restlichen Halbzellen wiederholen.
- Die gemessenen Werte von zwei weiteren Gruppen übernehmen und den Mittelwert berechnen.
Messungen
Vorlage.3
Entsorgen und Aufräumen
-
Die Flüssigkeiten mit Hilfe der Tropfflaschen aufsaugen. Überschüssige Lösungen in den Entsorgungsbehälter für Schwermetalle geben.
-
Alle verunreinigte Labormaterialien spülen und trocknen! Metall-Bleche blank schmirgeln.
-
Alle Materialien an ihren Ursprungsort zurückstellen.
M3
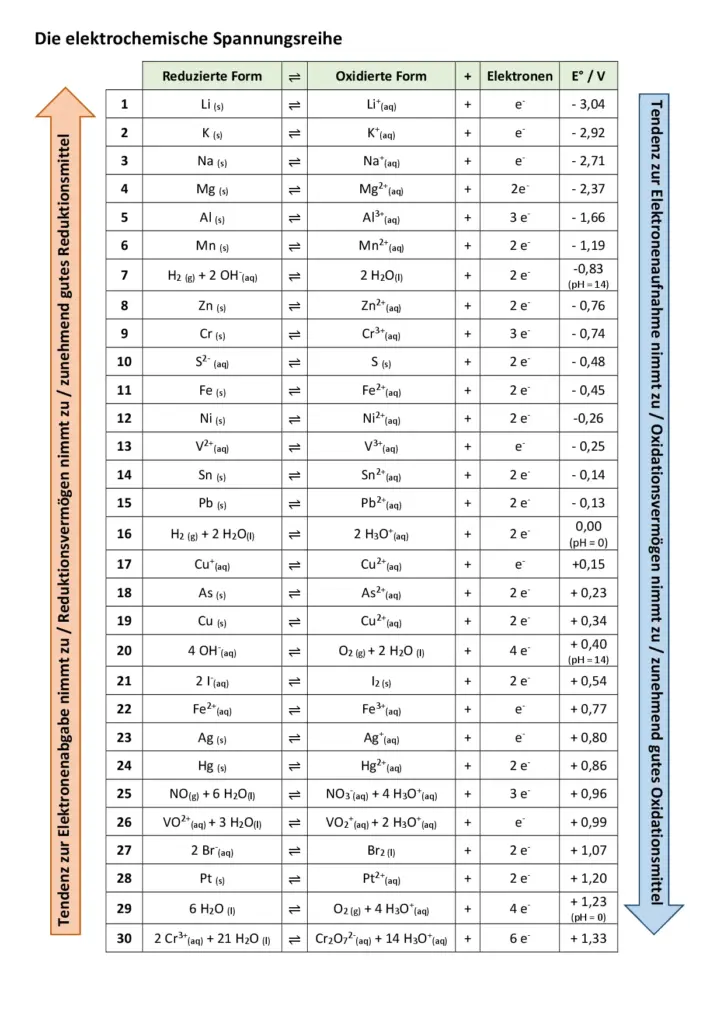
Eine umfangreiche elektrochemische Spannungsreihe
Weiteres
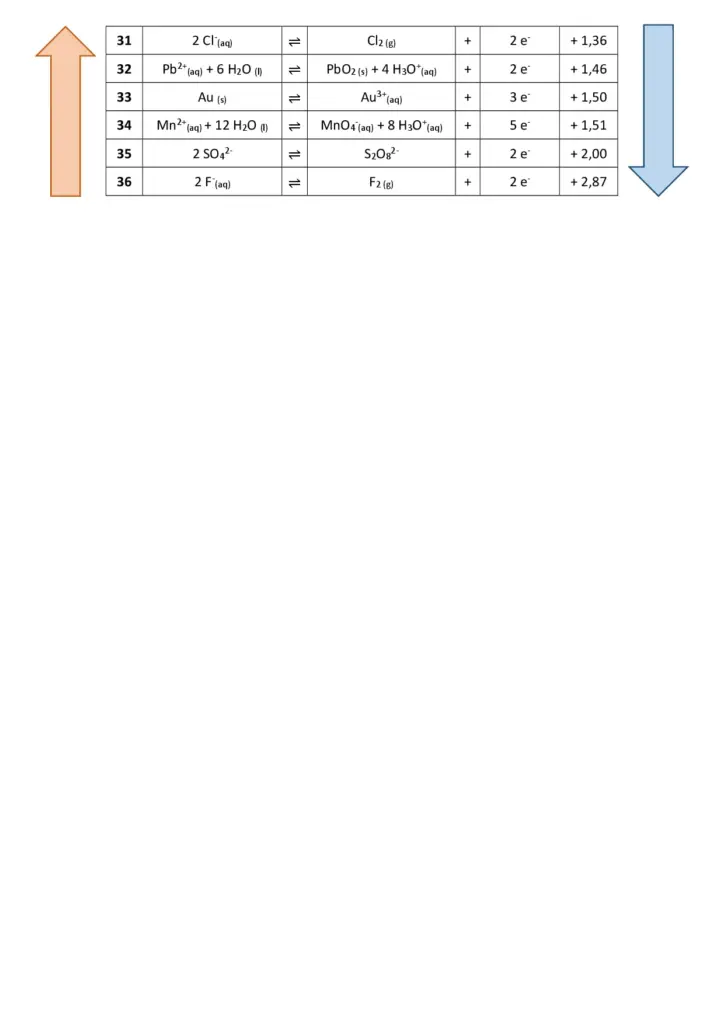
Eine umfangreiche elektrochemische Spannungsreihe.3
Aufgaben
- Korrigieren Sie, sofern notwendig, die Schreibweise der folgenden Zelldiagramme und berechnen Sie die zu erwartende Zellspannung unter Standardbedingungen.
- Cu2+/Cu // Ag+/Ag
- Fe/Fe2+ // Cu2+/Cu
- Zn/Zn2+ // Fe2+/Fe
- Bei der Herstellung von Platinen wird Kupfer geätzt. Hierfür kann Eisen-(III)-chlorid-Lösung verwendet werden. Erläutern Sie anhand der Redoxpotenziale, welche Reaktion dort abläuft. Ermitteln Sie, ob man auch eine Eisen-(II)-chlorid-Lösung zum Ätzen von Kupfer verwenden könnte.
- Begründen Sie, warum man für die Chlorhalbzelle nicht Platin, sondern Graphit als inert-Elektrode verwendet.