Was solltest du gelernt haben?
Weiteres
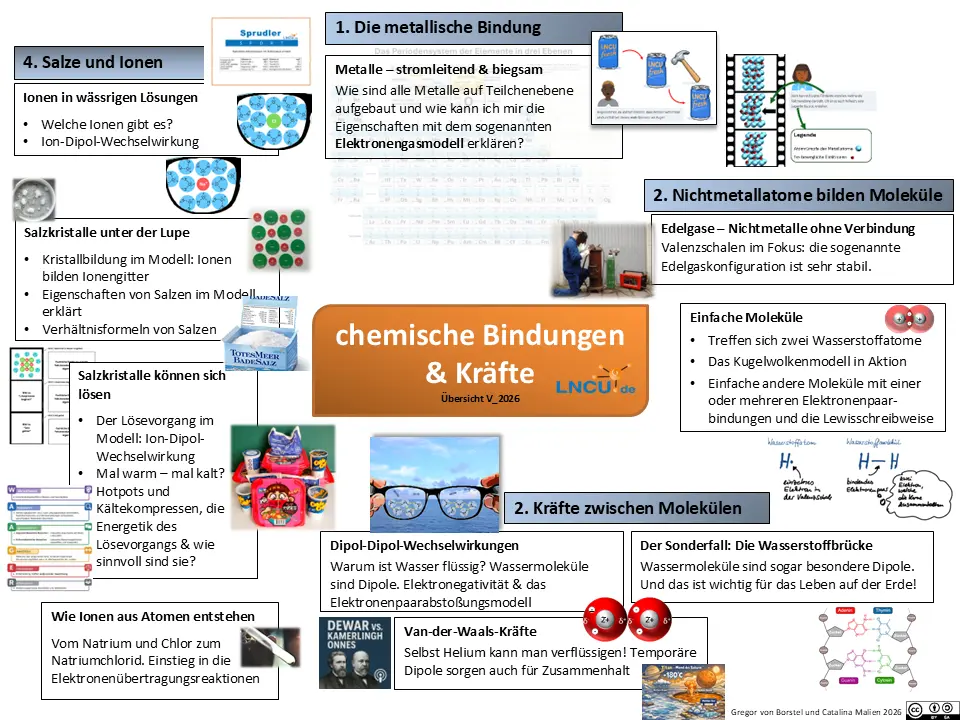
Ein Rückblick in Form eines Organizers.1
Weiteres
In diesem Kapitel hast du nicht einfach „Gruppen von Stoffen“ kennengelernt oder dich mit „Bindungstypen“ bekannt gemacht.
Du hast gelernt, Eigenschaften von Stoffen aus ihrem inneren Aufbau heraus zu erklären, chemische Prozesse auf Teilchenebene und symbolisch zu erläutern und damit kannst du nun ein stückweit bewusster mitreden, wenn es gilt, Fakten oder Vorgänge zu bewerten oder zu beurteilen.
Weiteres
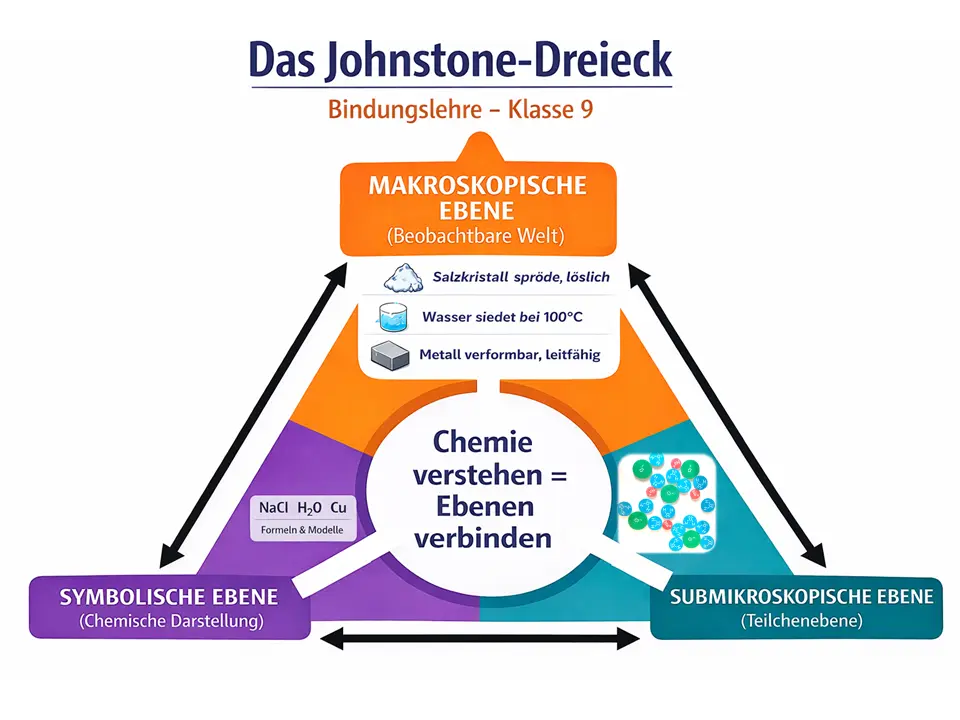
Die drei Ebenen, in denen ein Erläutern und Verständigung darüber funktionieren.2
Was solltest du im Einzelnen können
1. Bindungstypen benennen
Du kannst aus der Formel eines Stoffes mit Hilfe des PSE³ ableiten:
- Ist es ein Metall? Liegt ein Metallgitter vor?
- Besteht der Stoff aus Molekülen?
- Oder handelt es sich um ein Salz und liegt ein Ionengitter vor?
Beispiele: Du erkennst
- Mg als Formel für ein Metall (Magnesium), weil laut PSE³ Mg zu den Metalle gehört,
- H2O als die Summenformel für ein Molekül (Wasser), da es laut PSE nur aus Nichtmetallatomen besteht, die Elektronenpaarbindungen eingehen und
- NaCl als die Verhältnisformel eines Salzes (Natriumchlorid), das aus Metall-Kationen und Nichtmetall-Anionen aufgebaut ist, die ein Ionengitter bilden.
Übung
Analysiere und benenne, welche Bindungstypen den Substanzen mit folgenden Formeln vorliegen: Aluminium (Al), Aluminiumoxid (Al2O3), Ammoniak (NH3)
Anregungen
Suche „Al“ im Periodensystem. Bestimme, ob es als Metall oder Nichtmetall deklariert ist.
Aluminium (Al) gehört zu den Metallen, Sauerstoff (O) zu den Nichtmetallen. Was bedeutet dies automatisch für eine Verbindung aus solchen Stoffen?
Stickstoff und Wasserstoff sind Nichtmetalle. Ihre Atome verbinden sich über Elektronenpaarbindungen. Wie müsste das Molekül aussehen?
2. Eigenschaften mit Strukturen erklären
Du kannst Eigenschaften aus der Struktur begründen und dabei zwischen Beobachtung und Teilchenebene wechseln.
Das bedeutet, du kannst …
- eine beobachtbare Eigenschaft nennen
- eine Erklärung dafür auf Teilchenebene mit einer passenden Darstellung (Formel, Modell) geben.
Beispiel: Ein Salz ist hart (Beobachtung), da es aus einem regelmäßigen Ionengitter aus entgegengesetzt geladenen Ionen (Teilchenebene) aufgebaut ist.
Übung
3. Molekülstrukturen erkennen
Du kannst
- Lewis-Formeln von Molekülen zeichnen, dabei freie Elektronenpaare berücksichtigen und so Molekülgestalten vorhersagen,
- mit Hilfe der Elektronegativität die Bindungspolarität bestimmen
- mit der räumlichen Anordnung und Bindungspolarität die Polarität des Moleküls modellhaft bestimmen.
Beispiele: Du zeichnest eine korrekte Molekülgestalt eines Wassermoleküls, erklärst die Polarität der Bindung zwischen einem Wasserstoffatom und Sauerstoffatom, schlussfolgerst, dass ein Wassermolekül ein Dipol ist.
Übung
Zeichne ein Ammoniakmolekül (NH3). Bestimme, ob es sich um einen Dipol handelt.
Anregungen
4. Struktur -> Wechselwirkung -> Eigenschaft
Du kannst
- basierend auf der Polarität eines Moleküls die zwischenmolekularen Wechselwirkungen (Van-der-Waals-Kräfte, Dipol-Dipol-Wechselwirkungen, Wasserstoffbrücken) zwischen mehreren dieser Sorte benennen und
- die unterschiedlichen Siedetemperaturen damit erklären.
Beispiele: Du erkennst, dass Wassermoleküle permanente Dipole sind und aufgrund ihres besonderen Aufbaus sogar Wasserstoffbrücken untereinander ausbilden. Sauerstoffmoleküle hingegen sind keine permanenten Dipole und bilden untereinander nur Van-der-Waals-Kräfte aus. Wasser hat eine deutlich höhere Siedetemperatur als Sauerstoff.
Übung
Ammoniaktransport per Schiff.3
Wasserstoff (H2) gilt als klimafreundlicher Energieträger. Er kann nachhaltig mit Hilfe von Strom aus Wasser gewonnen werden. Dies gelingt besonders effizient in Ländern mit starker Sonneneinstrahlung. Allerdings ist Wasserstoff schwer zu transportieren, denn als als Gas würde er zu viel Raum einnehmen. Er wird aber erst bei −253 °C flüssig.
Ammoniak (NH3) wird als Alternative diskutiert. Es lässt sich aus Wasserstoff (H2) und Stickstoff (N2) herstellen, bei −33 °C verflüssigen und kann am Zielort wieder in Stickstoff und Wasserstoff (H₂) zerlegt werden
Erkläre, welche Rolle die Moleküleigenschaften von Ammoniak und Wasserstoff für die unterschiedliche Siedetemperaturen der Stoffe spielen.
Anregungen und Lösungen
Berechne die Elektronegativitätsdifferenz der Bindungen von
H–H und N–H (EN-Werte: H = 2,1; N = 3,0) und ordne die Bindungen als polar oder unpolar ein.
Beschreibe die räumliche Struktur von NH₃ mithilfe des EPA-Modells. (Tipp: Wie viele Elektronenpaare am Stickstoff?)
Erkläre, warum NH3 ein Dipolmolekül ist. Gehe dabei auf: Elektronegativität und Geometrie und
resultierenden Dipol ein.
Erkläre, warum H2 kein Dipolmolekül ist.
Erkläre mithilfe deiner Ergebnisse, warum Ammoniak leichter verflüssigt werden kann als Wasserstoff. Formuliere in wenigen Sätzen einen Zusammenhang zwischen:
- Polarität
- zwischenmolekularen Kräften
- Siedetemperatur
Die N–H Bindung ist wegen der EN-Differenz von 0,9 → polar
H2: gleiche Atome, symmetrische Ladungsverteilung, kein permanenter Dipol
NH3: 3 Bindungselektronenpaare; 1 freies Elektronenpaar; trigonal-pyramidale Struktur; unsymmetrische Ladungsverteilung; resultierender Dipol
H2: gleiche Atome, symmetrische Ladungsverteilung, kein permanenter Dipol
Wichtige fachliche Punkte:
NH3 ist polar → Dipol-Dipol-Wechselwirkungen, hier sogar Wasserstoffbrücken → stärkere zwischenmolekulare Kräfte → höhere Siedetemperatur (−33 °C)
H2 ist unpolar → nur Van-der-Waals-Kräfte → kleines Molekül, sehr schwache Anziehung → extrem niedriger Siedepunkt (−253 °C)
Zentraler Zusammenhang:
Je stärker die zwischenmolekularen Kräfte, desto höher die Siedetemperatur.
5. Lösen oder Kristallisation
Du kannst das Kristallisieren oder Lösen von Salzen als Prozess mit diversen Auswirkungen erläutern.
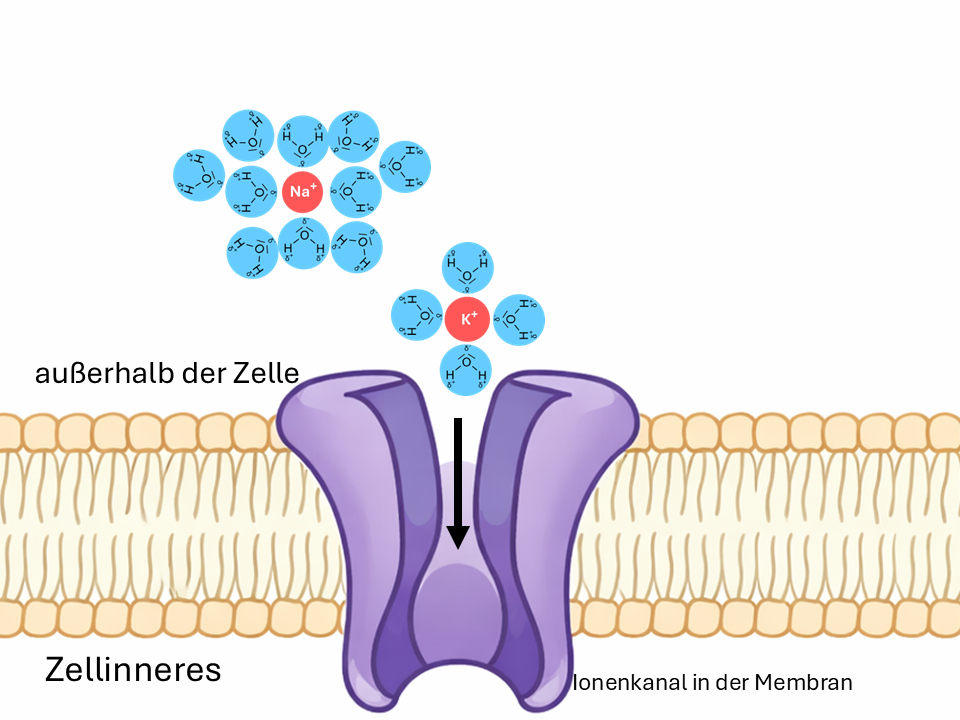
Beispiele: Du beschreibst, wie Salzlösungen auf Teilchenebene aussehen oder erklärst, warum kleinere Natrium-Ionen aufgrund ihrer größeren Hydrathülle mitunter schlechter Membranen passieren können als die größeren Kalium-Ionen mit ihrer kleineren Hydrathülle.
Stark vereinfachte Darstellung des Beispiels.4
Du beschreibst das Lösen von Salzen als Prozess (Aufbrechen des Ionengitters, Ionen-Dipol-Wechselwirkungen bis hin zur Hydratation der Ionen, Energieaspekte) und erläuterst, warum eine Kühlkompresse kalt wird.
Übung 1: Fehlersuchbild
Suche, benenne und korrigiere die Fehler im Fehlersuchbild.
Übung 2: Entstehung von Salzlagerstätten
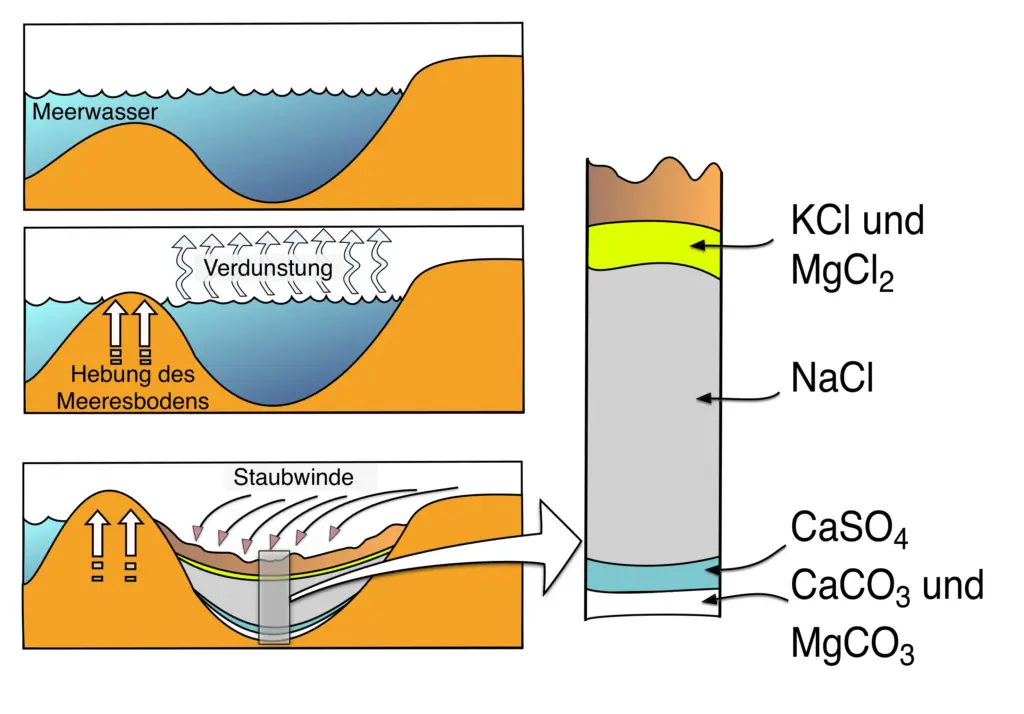
Entstehung einer Salzlagerstätte5
Aufgabenstellung
- Gib für alle in Tabelle 2 aufgeführten Salze die Formelschreibweise an.
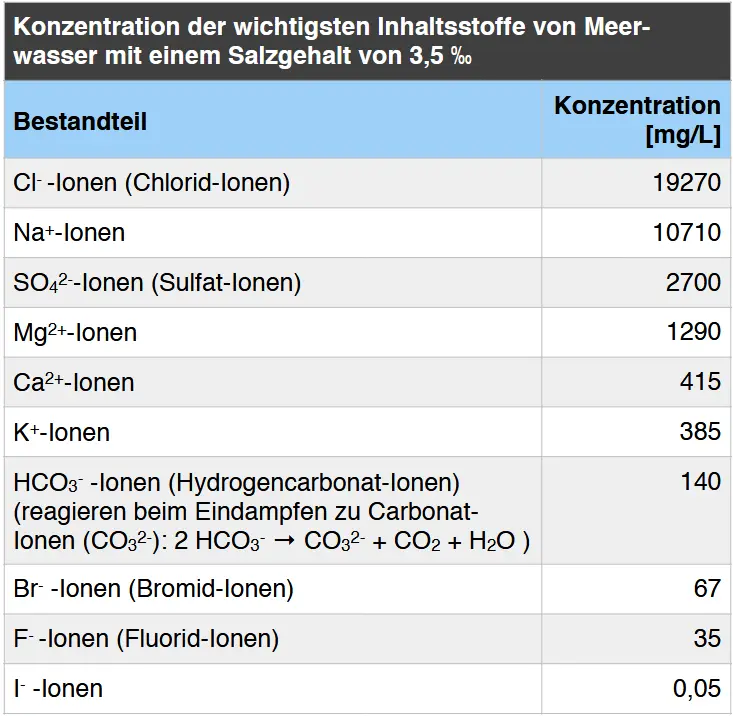
- Erkläre mit Hilfe der Tabelle 1 und Tabelle 2 das Zustandekommen der in Abb. 5 dargestellten Schichtung der Salze.
- Erkläre, warum in den hier erfassten Salzlagerstätten kein Natriumsulfat oder Natriumcarbonat vorkommt.
Konzentration ausgewählter Salze in Meerwasser5
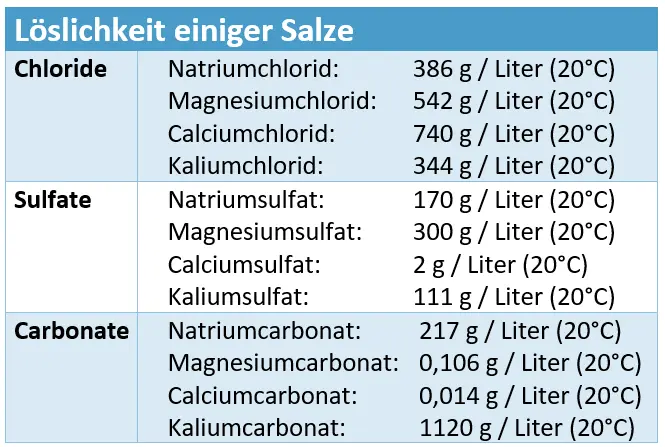
Löslichkeit ausgewählter Salze5
Lösungen
Chloride
- Natriumchlorid: NaCl
- Magnesiumchlorid: MgCl2
- Calciumchlorid: CaCl2
- Kaliumchlorid: KCl
Sulfate
- Natriumsulfat: Na2SO4
- Magnesiumsulfat: MgSO4
- Calciumsulfat: CaSO4
- Kaliumsulfat: K2SO4
Carbonate
- Natriumcarbonat: Na2CO3
- Magnesiumcarbonat: MgCO3
- Calciumcarbonat: CaCO3
- Kaliumcarbonat: K2CO3
aber nicht mit Na2CO3 oder Na2SO4.
Meerwasser enthält verschiedene Ionen, zum Beispiel Na+, Cl–, Ca2+, Mg2+, SO42- und HCO3–. Wenn Meerwasser in flachen Meeresbecken verdunstet, wird immer mehr Wasser entfernt. Dadurch steigt die Konzentration der gelösten Ionen. Sobald die Lösung mit einem bestimmten Salz gesättigt ist, beginnt dieses Salz auszufallen.
Die Reihenfolge der Ausfällung hängt vor allem von der Löslichkeit der Salze ab. Schwer lösliche Salze fallen zuerst aus, gut lösliche Salze erst später.
Schrittweise Erklärung der Schichtung
1. Zuerst fallen Carbonate aus
Im Meerwasser ist Hydrogencarbonat enthalten. Beim Eindampfen kann daraus Carbonat entstehen:
2 HCO3– → CO32- + CO2 + H₂O
Die Carbonat-Ionen reagieren mit Calcium- und Magnesium-Ionen. Da Calciumcarbonat (CaCO3) und Magnesiumcarbonat (MgCO3) nur wenig löslich sind, fallen sie zuerst aus. Deshalb liegen diese Salze in der Salzlagerstätte ganz unten.
2. Danach fällt Calciumsulfat aus
Wenn ein großer Teil der Carbonate bereits ausgefallen ist, bleiben weiterhin Calcium-Ionen und Sulfat-Ionen in Lösung. Calciumsulfat (CaSO4) ist ebenfalls nur begrenzt löslich und fällt deshalb als nächstes aus. Es bildet die nächste Schicht.
3. Danach fällt Natriumchlorid aus
Natriumchlorid (NaCl) ist besser löslich als Calciumcarbonat und Calciumsulfat. Es bleibt daher länger in Lösung und kristallisiert erst bei stärkerer Eindampfung. Deshalb bildet NaCl eine darüberliegende Schicht.
4. Zuletzt fallen sehr gut lösliche Chloride aus
Kaliumchlorid (KCl) und besonders Magnesiumchlorid (MgCl2) sind gut löslich. Sie bleiben am längsten in Lösung und fallen daher erst ganz am Ende aus. Deshalb liegen sie in den obersten Schichten.
Zusammenfassung
Die Schichtung entsteht also dadurch, dass beim Verdunsten des Meerwassers die Salze nacheinander entsprechend ihrer Löslichkeit ausfallen:
- zuerst schwer lösliche Carbonate,
- dann Calciumsulfat,
- dann Natriumchlorid,
- zuletzt gut lösliche Kalium- und Magnesiumchloride.
Aufgabe 1
Gib für alle in M3 aufgeführten Salze die Formelschreibweise an.
Chloride
Natriumchlorid: NaCl
Magnesiumchlorid: MgCl₂
Calciumchlorid: CaCl₂
Kaliumchlorid: KCl
Sulfate
Natriumsulfat: Na₂SO₄
Magnesiumsulfat: MgSO₄
Meerwasser enthält verschiedene Ionen, zum Beispiel Na+, Cl–, Ca2+, Mg2+, SO42- und HCO3–. Wenn Meerwasser in flachen Meeresbecken verdunstet, wird immer mehr Wasser entfernt. Dadurch steigt die Konzentration der gelösten Ionen. Sobald die Lösung mit einem bestimmten Salz gesättigt ist, beginnt dieses Salz auszufallen.
Die Reihenfolge der Ausfällung hängt vor allem von der Löslichkeit der Salze ab. Schwer lösliche Salze fallen zuerst aus, gut lösliche Salze erst später.
Schrittweise Erklärung der Schichtung
1. Zuerst fallen Carbonate aus
Im Meerwasser ist Hydrogencarbonat enthalten. Beim Eindampfen kann daraus Carbonat entstehen:
2 HCO3– → CO32- + CO2 + H₂O
Die Carbonat-Ionen reagieren mit Calcium- und Magnesium-Ionen. Da Calciumcarbonat (CaCO3) und Magnesiumcarbonat (MgCO3) nur wenig löslich sind, fallen sie zuerst aus. Deshalb liegen diese Salze in der Salzlagerstätte ganz unten.
2. Danach fällt Calciumsulfat aus
Wenn ein großer Teil der Carbonate bereits ausgefallen ist, bleiben weiterhin Calcium-Ionen und Sulfat-Ionen in Lösung. Calciumsulfat (CaSO4) ist ebenfalls nur begrenzt löslich und fällt deshalb als nächstes aus. Es bildet die nächste Schicht.
3. Danach fällt Natriumchlorid aus
Natriumchlorid (NaCl) ist besser löslich als Calciumcarbonat und Calciumsulfat. Es bleibt daher länger in Lösung und kristallisiert erst bei stärkerer Eindampfung. Deshalb bildet NaCl eine darüberliegende Schicht.
4. Zuletzt fallen sehr gut lösliche Chloride aus
Kaliumchlorid (KCl) und besonders Magnesiumchlorid (MgCl2) sind gut löslich. Sie bleiben am längsten in Lösung und fallen daher erst ganz am Ende aus. Deshalb liegen sie in den obersten Schichten.
Zusammenfassung
Die Schichtung entsteht also dadurch, dass beim Verdunsten des Meerwassers die Salze nacheinander entsprechend ihrer Löslichkeit ausfallen:
- zuerst schwer lösliche Carbonate,
- dann Calciumsulfat,
- dann Natriumchlorid,
- zuletzt gut lösliche Kalium- und Magnesiumchloride.
Natriumsulfat und Natriumcarbonat kommen in diesen Salzlagerstätten nicht vor, weil sich stattdessen andere, schlechter lösliche Salze bilden und früher ausfallen.
Begründung für Natriumcarbonat
Im Meerwasser reagieren Carbonat-Ionen nicht bevorzugt mit Natrium-Ionen, sondern vor allem mit Calcium-Ionen und Magnesium-Ionen, weil Calciumcarbonat und Magnesiumcarbonat deutlich schlechter löslich sind als Natriumcarbonat. Deshalb werden die Carbonat-Ionen bereits als Calcium- bzw. Magnesiumcarbonate aus der Lösung entfernt. Für die Bildung von Natriumcarbonat bleibt damit kaum Carbonat übrig.
Begründung für Natriumsulfat
Auch Sulfat-Ionen reagieren bevorzugt mit Calcium-Ionen, weil Calciumsulfat deutlich schlechter löslich ist als Natriumsulfat. Daher fällt Sulfat zuerst als Calciumsulfat aus. Das gut lösliche Natriumsulfat bleibt nicht als eigenes Lagerstättensalz zurück.
Gesamterklärung
Ob ein Salz in einer Salzlagerstätte entsteht, hängt nicht nur davon ab, ob seine Ionen im Meerwasser vorkommen, sondern auch davon, welche Kombination der Ionen das schwerer lösliche Salz bildet. Die schwerer löslichen Calcium- und Magnesiumsalze fallen früher aus.
6. Chemische Zusammenhänge bewerten
Du kannst das WAAGE(R)-Modell nutzen und damit ein begründetes Urteil formulieren.
Beispiel: Du kannst ein Problem wie die Frage, ob ein Hotpot oder eine Kühlkompresse etwas Sinnvolles oder Quatsch sind, wahrnehmen und analysieren, du findest Argumente, gewichtest sie und triffst begründete Entscheidungen. Du reflektierst dein Vorgehen.
Übung
Nehmen wir das Beispiel „Streusalz im Winter – sinnvoll oder problematisch?“. Du musst ja nicht den ganzen WAAGE(R)-Prozess durchlaufen. Lass uns mal beginnen.
Nimm das Problem wahr und benenne das Dilemma hinter der Frage. Analysiere, was du wissen müsstest und suche nach Kriterien, die wichtig sein könnten.
Anregungen und Lösungen
Es geht um Verkehrssicherheit vs. Umweltschäden
- Gefrierpunktserniedrigung – Salzlösungen haben einen niedrigeren Gefriepunkt als Wasser, folglich sind Salzlösungen auch bei geringeren Temperaturen noch flüssig
- Salzlösungen gelangen von der Straße in die Umgebung und haben einen schädigenden Einfluss auf Böden & Pflanzen
- Es kommt zudem zur verstärkten Korrosion von Metallen
Mögliche Kriterien, die man zu Argumenten ausbauen kann
- Sicherheit
- Umweltbelastung
- Materialschäden
- Alternativen (Splitt, Sand)
7. Ionenbildung beschreiben
Du kannst mit Hilfe des Periodensystems beschreiben, welche Anionen oder Kationen ausgewählte Elemente bilden und kannst eine Elektronenübertragungsreaktion in Form von Reaktionsgleichungen schreiben.
Und die kennst die Triebkraft hinter der Reaktionen
Es bilden sich genau diese Ionen, das volle Schalen verhältismäßig stabil sind und das Entfernen oder Hinzufügen weiterer Elektronen viel mehr Energie benötigen würde.
Der Prozess führt zu einem stabilen Zustand, weil bei der Ionengitterbildung schlussendlich viel Energie frei wird.
Beispiel: Du weißt, dass durch eine Elektronenübertragungsreaktion aus einem Natrium-Atom ein Natrium-Ion und zugleich aus einem Chloratom ein Chlorid-Ion werden.
Übung
Stelle dar, welches Salz sich aus Magnesium und Brom bilden sollte.