Reaktionen in (vorübergehend) geschlossenen Systemen
Weiteres
Was geschieht eigentlich mit den Konzentrationen von Stoffen, wenn man mehrere Edukte in einem geschlossenen Gefäß reagieren lässt und zunächst einmal kein Produkt entweicht?
Warum fragst du das?
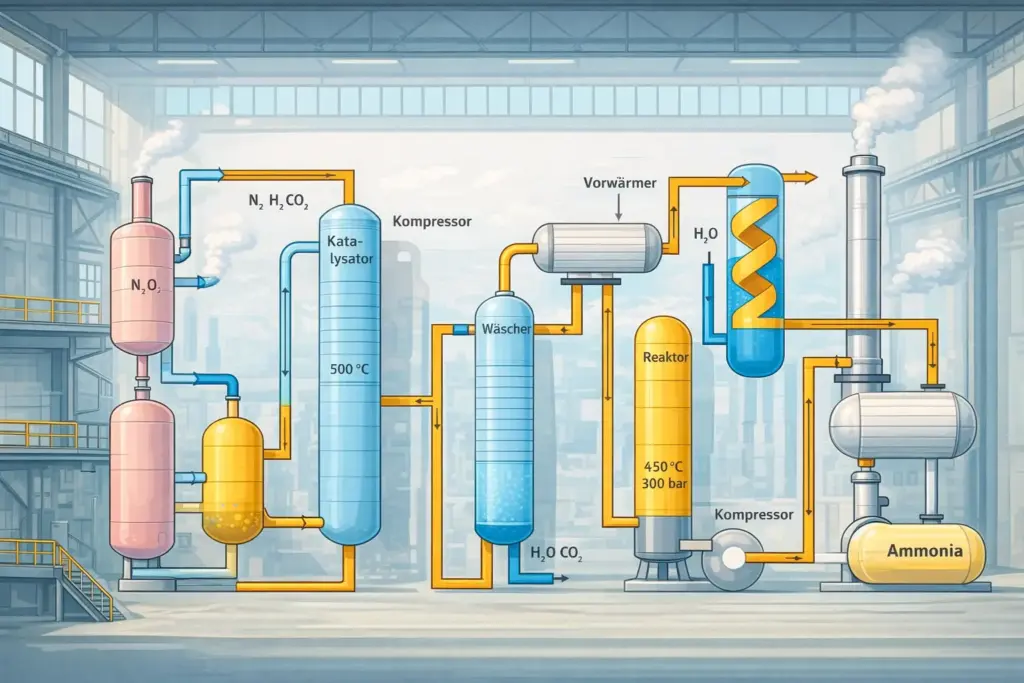
Es interessiert mich, denn in einer Zelle oder einer Fabrikanlage kann der Zufluss der Edukte oder der Abfluss der Produkte ja auch gesteuert werden.
Weiteres
Stimmt! Wenn man es genau betrachtet ist unsere Erde mit Atmosphäre, Lithosphäre, Technosphäre, Biosphäre und Hydrosphäre auch ein großes Gefäß.
Zelle, Anlage, Erde – alles keine ganz geschlossenen Systeme – aber dennoch mit einen „Deckel“ versehen1
Wir werden sehen, dass diese Frage interessante Antworten bereit hält. Vor allem, wenn wir ab und zu das Gefäß aufmachen, etwas verändern und die Prozesse damit beeinflussen.
Aufgaben
- Machen Sie sich mit dem Szenario des Experiments in M2 vertraut.
- Stellen Sie eine Hypothese auf, wie sich die Konzentrationen der Ethansäure in dem Szenario mit der Zeit nach unserem bisherigen Kenntnisstand vermutlich verändert.
Estersynthese im geschlossenen Gefäß
Weiteres
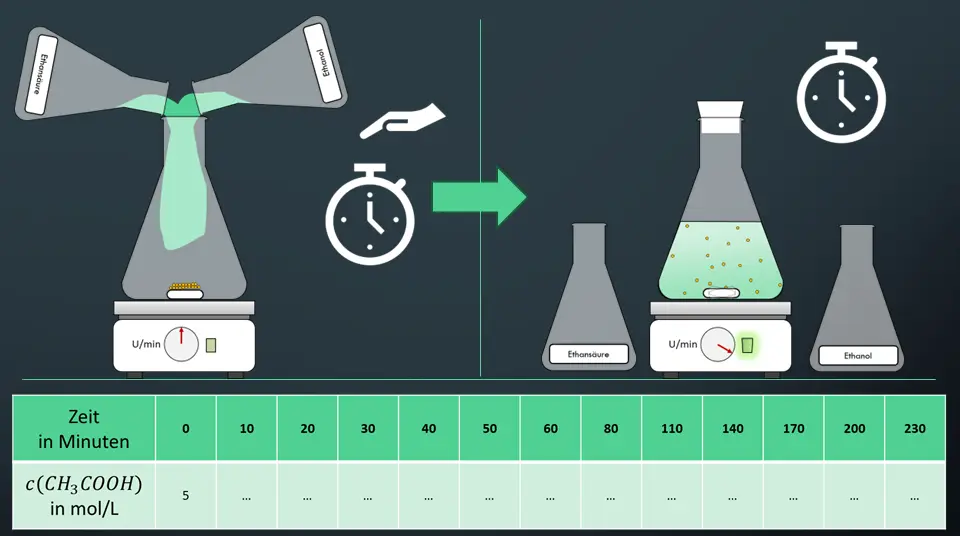
Wir stellen noch einmal Ethansäureethylester her. Der Unterschied zum letzten Mal: Wir machen sofort nach dem Zusammengeben der Edukte einen festen Stopfen auf das Gefäß und starten einen Timer.
Versuchsaufbau2
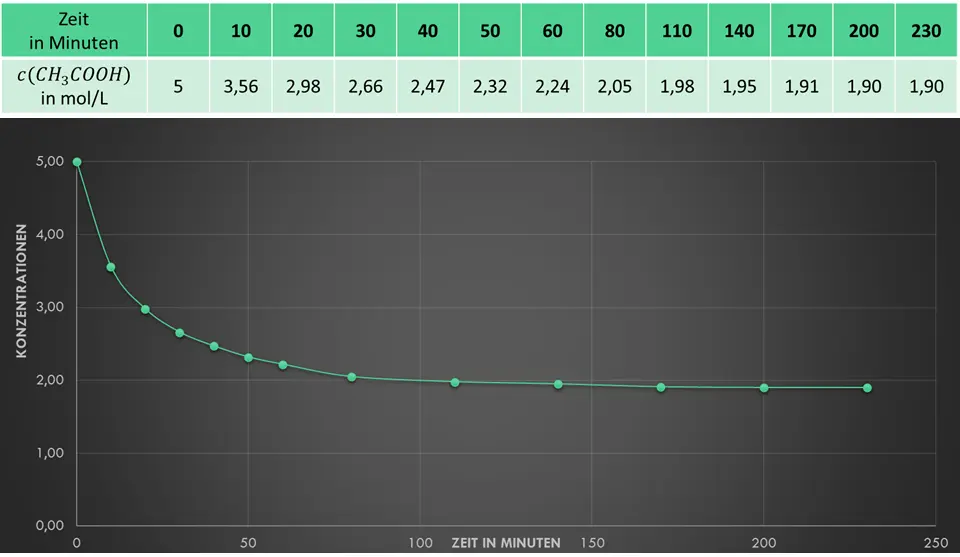
Die Anfangskonzentration der Ethansäure und die Anfangskonzentration von Ethanol sind gleich. Sie beträgt jeweils 5 mol/L.3. Damit ist sichergestellt, dass die gesamte Ethansäure reagieren kann.
Die gelben Kugeln in Abb. 1 stellen den sauren Ionentauscher dar, der die H+-Ionen liefert, die als Katalysator wirken.
Weiteres
Alle 10 Minuten stechen wir mit einer Kanüle durch den Stopfen, entnehmen eine winzige Probe und bestimmen die noch vorhandene Konzentration der Ethansäure.4.
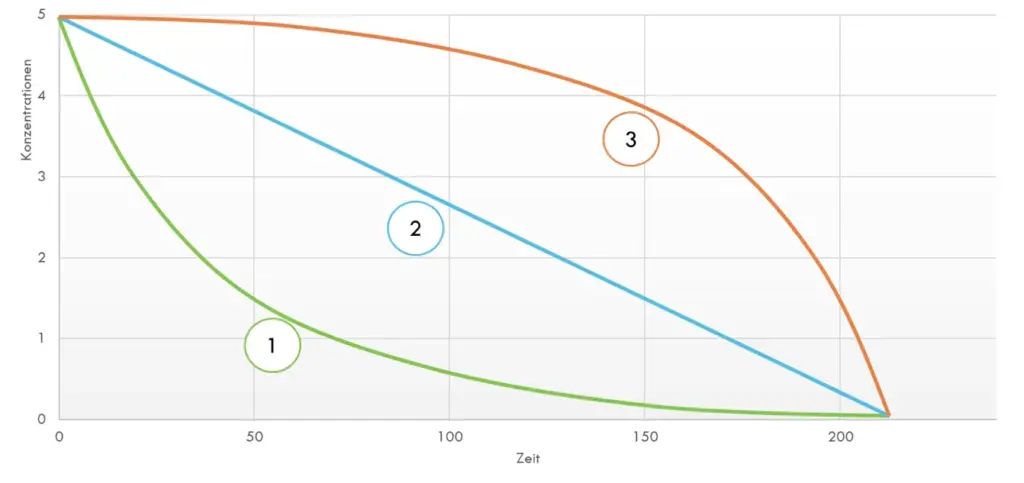
Denkbare Kurvenverläufe für die gemessene aktuelle Konzentration der Essigsäure.5
Was erwartest Du für einen Kurvenverlauf? 1, 2 oder 3? Oder eine andere Kurve? Dann beschreibe diese.
Aufgaben
-
Stellen Sie Gemeinsamkeiten und Unterschiede der Kurven in M2 und dem realen Verlauf in M3 heraus.
-
Entwickeln Sie Erklärungsansätze für die Abweichungen.
-
Nutzen Sie M3 als Informationsquelle zum Abgleich ihrer Erklärungen.
Reale Daten und ein Erklärungsansatz
Ein Erklärungsansatz
Wieso konvergiert die Konzentration der Salzsäure nicht gegen 0 mol/L?
Die Reaktion geht auch nach einiger Zeit immer weiter. Aber nun ist bereits ein merkliche Menge an Ethansäureethylester entstanden. Da die Moleküle aller Stoffe aber im Gefäß bleiben, stoßen auch entstehende Produktmoleküle zusammen.
Folglich bildet sich Ethansäure immer immer wieder neu!
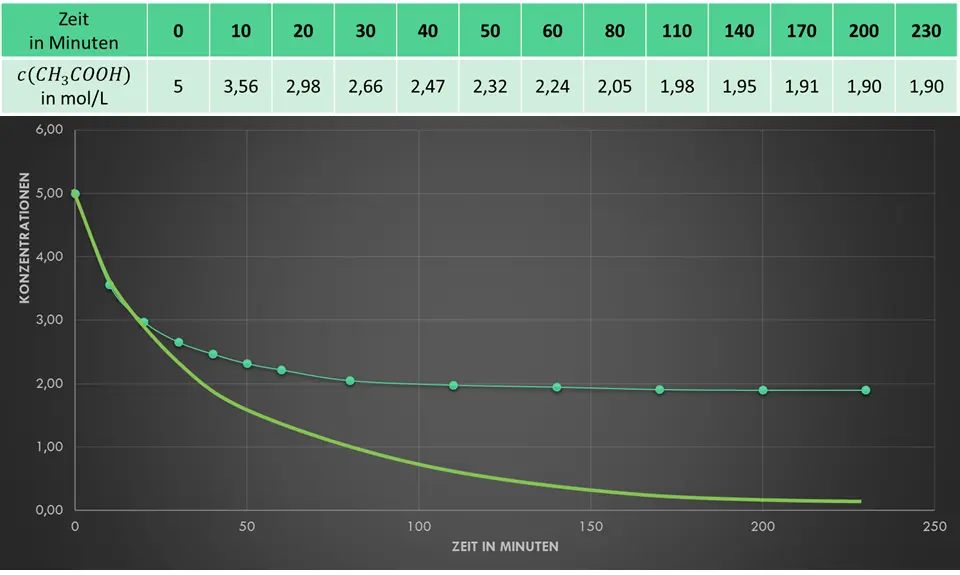
Du kannst es vielleicht besser sehen, wenn wir Kurven für die Konzentration des Ethansäureethylester mit in das Diagramm aufnehmen.
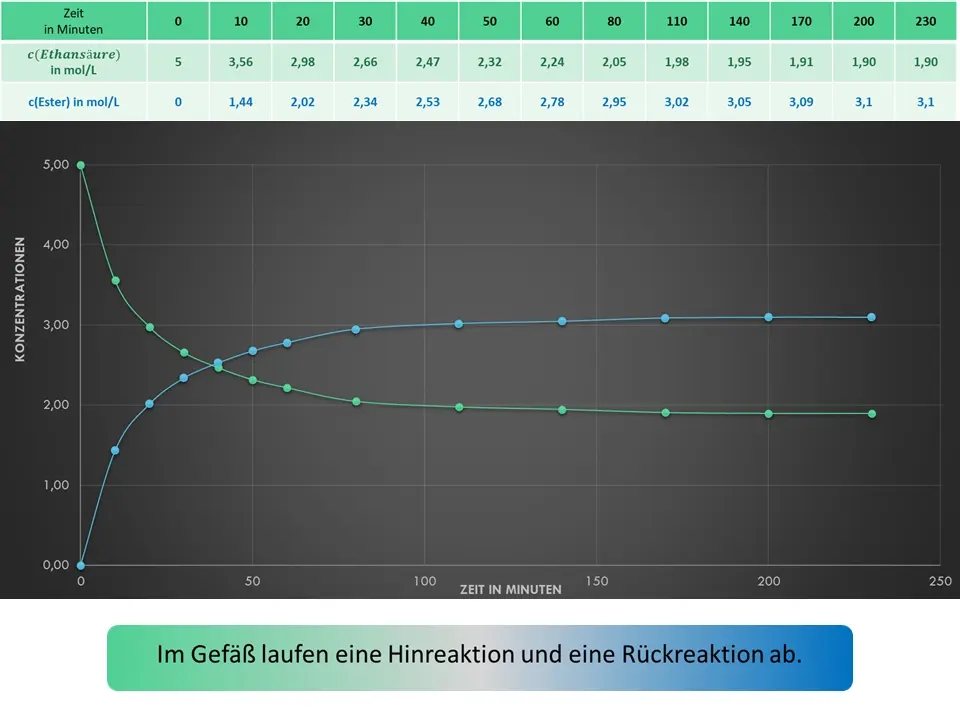
Es laufen also eine Hinreaktion (Esterbildung) und eine Rückreaktion (Esterspaltung, Bildung von Ethansäure) ab!
Dies kann man durch einen doppelten Pfeil zum Ausdruck bringen.
Schau einmal in die Wertetabelle und in das Diagramm. Ab einem gewissen Zeitpunkt verändern sich die Konzentrationen der Stoffe nicht mehr. Dann sind Hinreaktion und Rückreaktion gleichschnell.

Ein sogenanntes chemisches Gleichgewicht hat sich eingestellt. Dies bringt man durch einen besonderen Pfeil zum Ausdruck: den doppelten Harpunenpfeil.
Alles klar bis hierher?
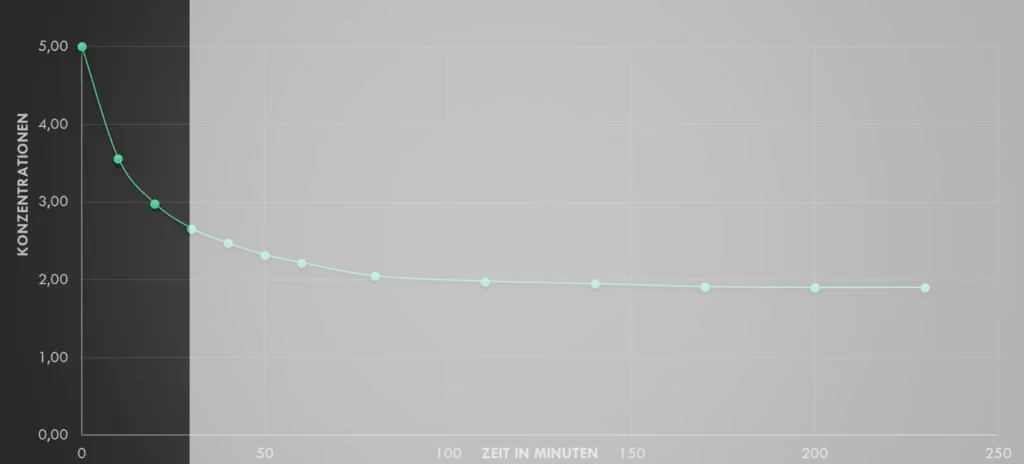
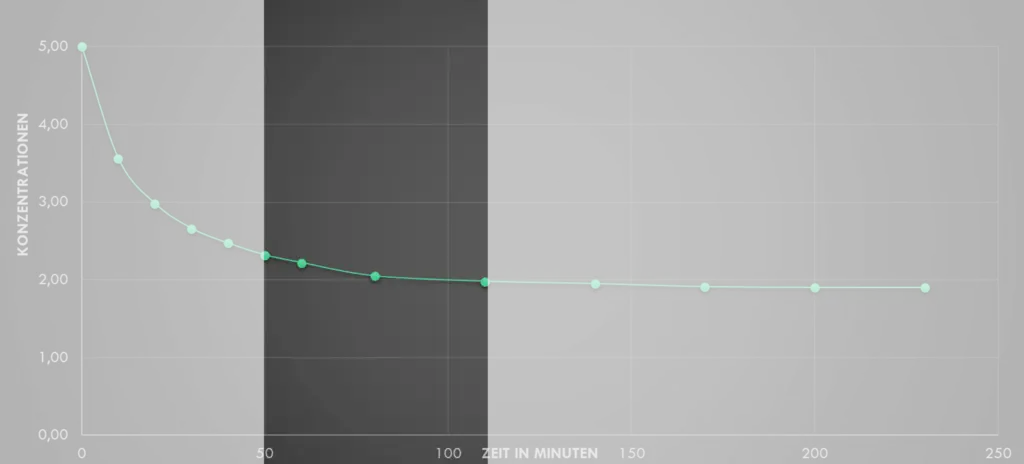
- Verschiebe den Schieberegler in M4 auf folgende Zeitpunkte im Verlauf der Reaktion und mache ein Bildschirmfoto:
- Die Konzentration an Ethansäure ist genauso groß wie die Konzentration an Ethansäureethylester.
- Pro Zeiteinheit werden genauso viele Essigsäure- und Alkoholmoleküle bei der Hinreaktion umgesetzt wie bei der Rückreaktion gebildet werden.
- Ein chemisches Gleichgewicht hat sich eingestellt.
Kurvenverläufe und Zeitpunkte
Weiteres