Katalysatoren gibt es viele – hier ein Beispiel
Wasserstoffperoxid ist gefährlich
Wasserstoffperoxid enthält wie alle Peroxide eine Sauerstoff-Sauerstoff-Einzelbindung.
Dadurch ist es instabil und kann unter Sauerstoffabspaltung schon bei Raumtemperatur zerfallen.
Die Katalase schützt Zellen
Wasserstoffperoxid entsteht auch als Nebenprodukt bei vielen Stoffwechselreaktionen in Zellen unter anderem in Mitochondrien.
Wegen seiner hohen Reaktionsfreudigkeit könnte Wasserstoffperoxid in der Zelle z. B. im Zellkern Proteine oder Nucleinsäuren schädigen und muss daher möglichst schnell nach seiner Entstehung abgebaut werden.
Viele Lebewesen schützen sich gegen diese schädigende Wirkung von Wasserstoffperoxid, in dem sie das Enzym Katalase produzieren.
Bei Enzymen handelt es sich um Katalysatoren in Lebewesen. Katalase findet man sowohl in den Zellen von Tieren als auch in Pflanzenzellen oder Hefen. Es sorgt dafür, dass entstehendes Wasserstoffperoxid direkt abgebaut wird.
Wie kam das Problem in Zellen und was können wir tun?
Harshita Kaul & Roberta Colapietro stellen in ihrem science-slam-Beitrag „Mitochondria“ die Endosymbiontentheorie und die Problematik des Wasserstoffperoxids vor. Absolute Empfehlung in M3!
Wirkweise von Katalase aus Trockenhefe auf Wasserstoffperoxid
Materialien
- Schutzbrille
- Handschuhe
- Spatel
- Kelchglas
- Glimmspan
Chemikalien
- Wasserstoffperoxid-Lösung 5%
Weiteres
Um den Einfluss eines Katalysators (hier Katalase) auf die Geschwindigkeit einer chemischen Reaktion (hier Zerfall von Wasserstoffperoxid) einmal live zu beobachten, können wir einfach Trockenhefezelle in Wasserstoffperoxid tauchen. Die Flüssigkeit dringt in die Zellen ein und kommt mit Katalase in Kontakt.
Durchführung
- Füllen Sie 20 mL der Wasserstoffperoxid-Lösung in das Kelchglas und geben Sie einen Löffel Trockenhefe hinzu.
- Beobachten Sie kurz.
- Prüfen Sie durch Eintauchen des glimmenden Spans in den entstandenen Schaum, ob es sich beim entstehenden Gas tatsächlich um Sauerstoff handelt.
Entsorgen und Aufräumen
-
Reste in den Ausguss geben und mit viel Wasser nachspülen.
-
Alle verunreinigte Labormaterialien spülen.
-
Alle Materialien an ihren Ursprungsort zurückstellen.
Aufgaben
- Geben Sie einen Grund an, warum man Wasserstoffperoxid-Lösung im Kühlschrank aufbewahrt.
- Führen Sie den Versuch V1 durch und beschreiben Sie, inwiefern er die Wirkungsweise eines Katalysators demonstriert.
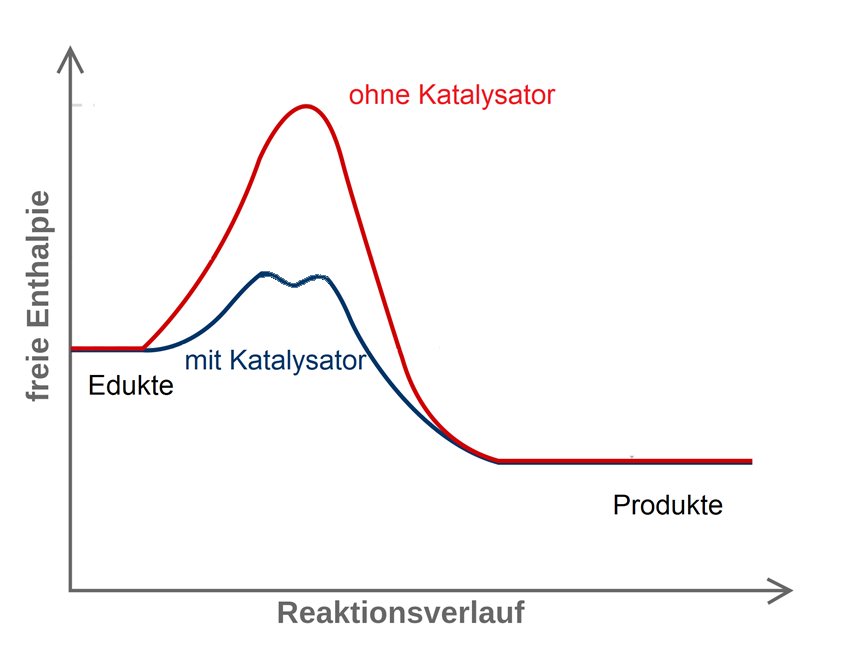
- Betrachten Sie die animierte Darstellung der Wirkweise von Katalase M2 und beschreiben Sie daraufhin das Energiediagramm für die Zersetzung von Wasserstoffperoxid mit und ohne Katalysator.
- Erläutern Sie den Einfluss eines Katalysators auf die Reaktionsgeschwindigkeit mit Hilfe der Boltzmann-Verteilung.
Hintergründe
Zum Enzym
Das Enzym Katalase enthält ein Eisen-Ion aus der „Häm“ Gruppe im aktiven Zentrum1. An dieses aktive Zentrum wird das H2O2-Molekül gebunden und kontrolliert gespalten.
Den Vorgang zeigt diese Animation modellhaft.
Ein Katalysator eröffnet andere Reaktionwege
Energiediagramm mit und ohne Katalysator im Vergleich.2
Weiteres
Total interessant
Mitochondria | Science Slam
Harshita Kaul & Roberta Colapietro3
Aus der Forschung
Die Max-Planck-Gesellschaft veröffentlich regelmäßig kostenlose Materialien aus der Forschung für interessierte Schülerinnen und Schüler.
Hier zwei Beispiele zu Katalysatoren:
- Nobelpreis für „Magische Moleküle“
- Katalyse zur Ammoniak (NH3) Spaltung und Nutzung als Wasserstoffspeicher.