Ausgangsgedanken
Weiteres
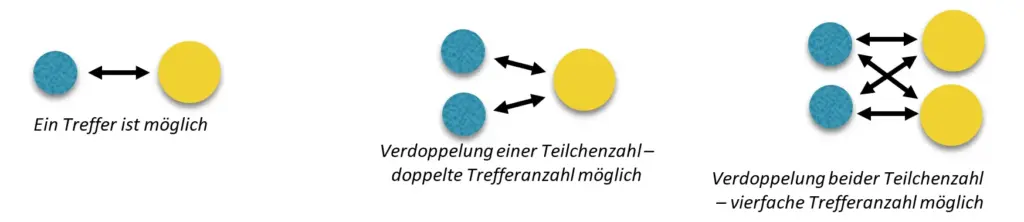
Basierend auf dem Modell der Stoßtheorie müssten doch logischerweise alle Reaktionsgeschwindigkeiten direkt proportional zu den Konzentrationen aller beteiligen Stoffe sein.
Weiteres
Die Verdopplung einer Teilchenzahl führt zur Verdopplung der Treffermöglichkeiten.1
Weiteres
Das stimmt eigentlich! Für die Reaktion A + B -> Produkt(en) mit A und B als Stoffe in einer Lösung sollte laut Modell für die Reaktionsgeschwindigkeit v stets gelten:
Solche Formeln nennt man ein Geschwindigkeitsgesetz.
Und für andere Reaktionen könnten ein „Geschwindigkeitsgesetz“ dann so aussehen:
Aufgaben
- Vollziehen Sie die Gedanken in M1 nach und erklären Sie die mathematische Darstellungen.
- Klären Sie in M2 alle Fachbegriffe und ergänzen Sie die noch fehlenden Reaktionsordnungen.
- Benennen Sie eine Reaktion, in welcher die Erwartung aus dem Modell M1 von den Messungen in der Wirklichkeit M2 abweichen.
- Erklären Sie basierend auf M3 die dort gezeigte Abweichungen von Erwartung laut Modell zu gemessener Realität.
- Modelle helfen beim Verständnis der Wirklichkeit. Beschreiben Sie einen falsche Nutzung von Modellen und einen korrekten Umgang mit Modellen, der sich aus der heutigen Betrachtung ergibt.
Messungen ergeben mitunter andere Geschwindigkeitsgesetze
Weiteres
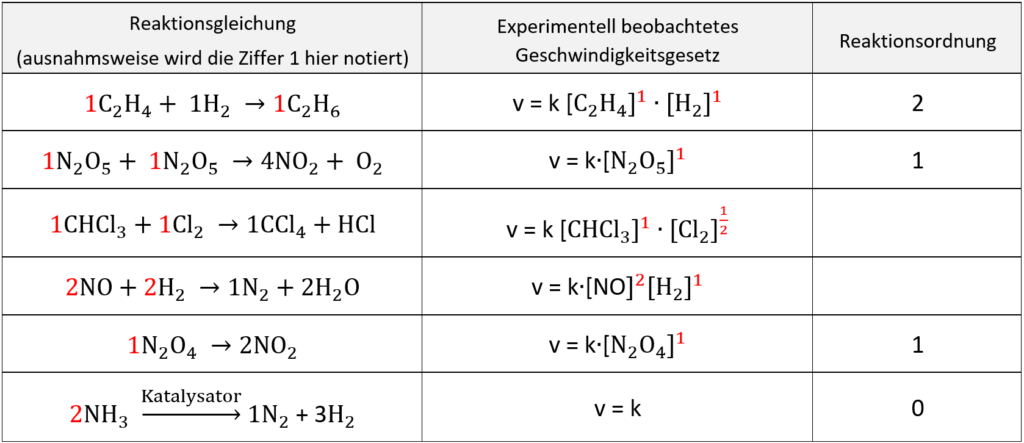
Reaktionsgleichungen, tatsächliches Geschwindigkeitsgesetz und Reaktionsordnung.2
Weiteres
Als Reaktionsordnung bezeichnet man die Summe aller Exponenten der Konzentrationen im Geschwindigkeitsgesetz.
Nicht alle Reaktionen haben eine Reaktionsordnung, die der Summe der stöchiometrischen Faktoren der Edukte in der Reaktionsgleichung entspricht, obwohl man dies nach dem einfachen Modell der Stoßtheorie erwarten würde.
Dies bedeutet, dass die Konzentrationen einiger Edukte mitunter weniger Einfluss auf die Geschwindigkeit der Reaktion haben als die Konzentrationen anderer Edukte.
Eine durchdachte Erklärung für die Abweichung
Weiteres
Chemische Reaktionen laufen nämlich selten in einem einzigen Schritt ab. Eine Gesamtreaktionsgleichung zeigt uns nur den Anfangs- und Endzustand einer chemischen Reaktion – also was wir hineingeben und was am Ende herauskommt. Die Elementarreaktionen dagegen beschreiben, was tatsächlich auf molekularer Ebene Schritt für Schritt passiert.
In der Regel weichen die Geschwindigkeitsgesetze von der Erwartung ab, wenn die Reaktionen nicht in einem Schritt ablaufen. Das bedeutet, dass es nicht immer so ist, dass zwei Eduktteilchen einfach aufeinanderprallen und daraus die Produkte entstehen.
Besteht eine Gesamtreaktion aus mehreren Reaktionsschritten, so bestimmt der langsamste Schritt – also die langsamste Elementarreaktion – die Geschwindigkeit der Gesamtreaktion. Damit sind nur die Konzentrationen der Stoffe relevant, die an den Reaktionen bis zum langsamsten Schritt beteiligt sind.
Beispiel:
Experimentell ermitteltes Geschwindigkeitsgesetz:
Weiteres
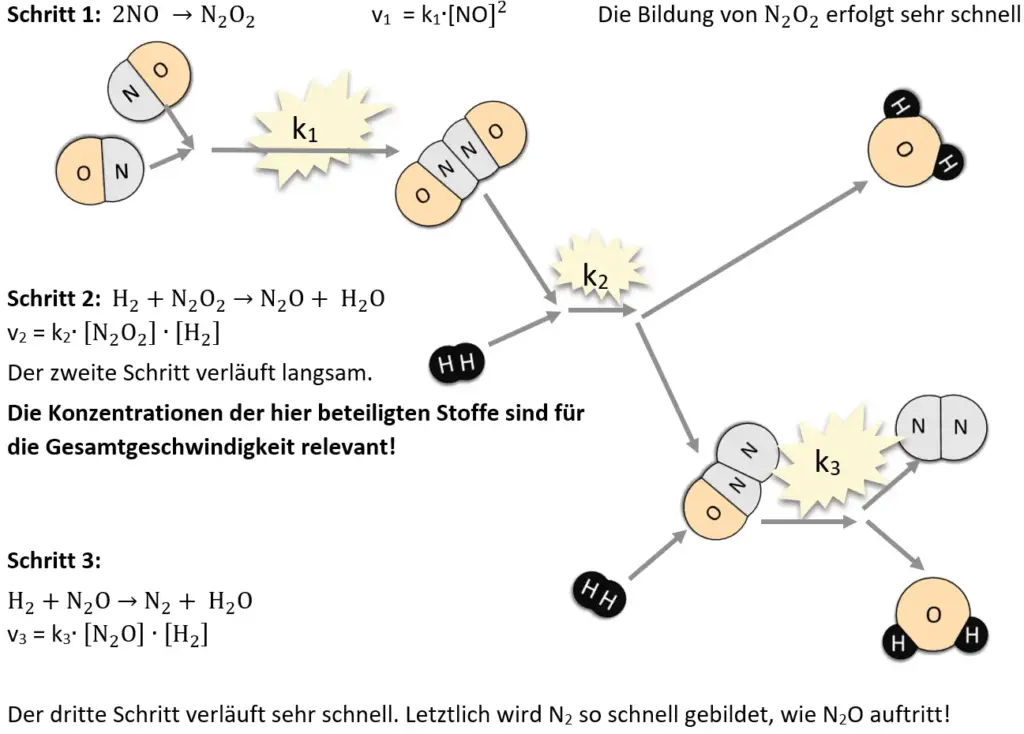
Die Reaktion ist nicht insgesamt 4. Ordnung bzw. 2. Ordnung bezüglich der Konzentration von H2. Sie verläuft daher sicherlich über einen mehrschrittigen Mechanismus. Die drei Elementarreaktionen könnten wie folgt aussehen:
Modellhafte Darstellung der Reaktion3
Aus einer Gesamtreaktionsgleichung kann man niemals das Geschwindigkeitsgesetz ableiten, da man nicht sicher weiß, ob es sich um eine Elementarreaktion handelt!
Ausblick auf den späteren Chemieunterricht: Mitunter hat die Konzentration der einen Edukte weniger Einfluss auf die Geschwindigkeit der Reaktion als die Konzentrationen anderer Edukte. Die experimentell bestimmte Reaktionsordnung kann dann Hinweise über den tatsächlichen Reaktionsmechanismus geben.
Weitergedacht
- Beschreiben Sie eine Vorgehensweise, mit der man in der Realität ein Geschwindigkeitsgesetz für eine beliebige Reaktion prinzipiell bestimmen könnte.